
科目: 来源:北京高考真题 题型:单选题
 Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是
Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是 查看答案和解析>>
科目: 来源:安徽省模拟题 题型:单选题
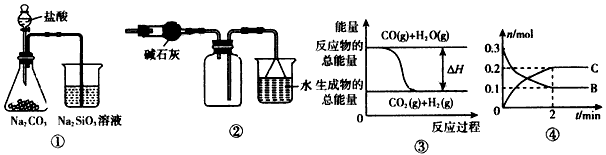
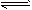 CO2(g)+H2(g)的△H>0
CO2(g)+H2(g)的△H>0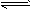 xC(g),根据图④可以求出x=2
xC(g),根据图④可以求出x=2 查看答案和解析>>
科目: 来源:海南省模拟题 题型:填空题
 H2(g)+CO2(g) △H=QkJ/mol,其平衡常数随温度的变化如下表
H2(g)+CO2(g) △H=QkJ/mol,其平衡常数随温度的变化如下表

查看答案和解析>>
科目: 来源:江苏模拟题 题型:填空题
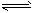 H2O(l)
H2O(l)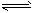 H2NCOONH4(氨基甲酸铵)(l) △H1
H2NCOONH4(氨基甲酸铵)(l) △H1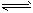 H2O(l)+H2NCONH2(l) △H2
H2O(l)+H2NCONH2(l) △H2 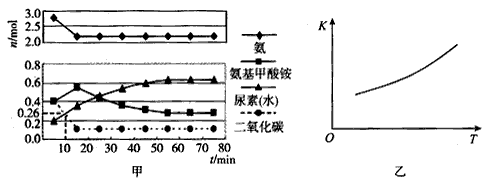
查看答案和解析>>
科目: 来源:河南省模拟题 题型:单选题
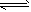 2C(g),若经2s后测得C的浓度为0.6mol/L,现有下列几种说法:
2C(g),若经2s后测得C的浓度为0.6mol/L,现有下列几种说法:查看答案和解析>>
科目: 来源:陕西省模拟题 题型:单选题
查看答案和解析>>
科目: 来源:专项题 题型:单选题
查看答案和解析>>
科目: 来源:专项题 题型:单选题

查看答案和解析>>
科目: 来源:湖南省模拟题 题型:单选题
查看答案和解析>>
科目: 来源:模拟题 题型:填空题
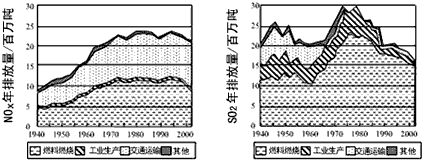
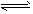 N2+2CO2将有害的污染物转化为可参与大气循环的N2和CO2。在某温度下用气体传感器测得不同时间的NO和CO浓度如下表
N2+2CO2将有害的污染物转化为可参与大气循环的N2和CO2。在某温度下用气体传感器测得不同时间的NO和CO浓度如下表
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com