
科目: 来源:同步题 题型:填空题
 2NH3是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1 mol H-H键、1 mol N-H键、1mol N三N键放出的能量分别为436 kJ、391 kJ、946 kJ。则:
2NH3是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1 mol H-H键、1 mol N-H键、1mol N三N键放出的能量分别为436 kJ、391 kJ、946 kJ。则:查看答案和解析>>
科目: 来源:同步题 题型:填空题

(1)该反应的反应物是_______,生成物是_______。
(2)该反应的化学方程式为________________。
(3)反应开始至2 min时,____(填“能”或“不能”)用物质C表示该反应的反应速率,若能,其反应速率为 _______,若不能,其原因是_________。
(4)2 min后,A、B、C的物质的量不再随时间的变化而变化,说明在这个条件下,该反应__________。
查看答案和解析>>
科目: 来源:0112 月考题 题型:单选题
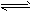 3C+4D(A、B、C、D均是气体)反应中,表示该反应速率最快的是
3C+4D(A、B、C、D均是气体)反应中,表示该反应速率最快的是查看答案和解析>>
科目: 来源:山东省高考真题 题型:填空题
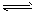 H2+I2
H2+I2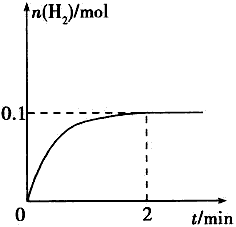
查看答案和解析>>
科目: 来源:0127 期中题 题型:计算题
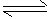 2SO3 (g)。若经过2s后测得SO3的浓度为0.6 mol/ L,
2SO3 (g)。若经过2s后测得SO3的浓度为0.6 mol/ L,查看答案和解析>>
科目: 来源:0103 期中题 题型:单选题
 4NO(g)+6H2O(g),在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率ν(X)(反应物的消耗速率或产物的生成速率)可表示为
4NO(g)+6H2O(g),在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率ν(X)(反应物的消耗速率或产物的生成速率)可表示为查看答案和解析>>
科目: 来源:同步题 题型:计算题
查看答案和解析>>
科目: 来源:期末题 题型:计算题
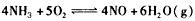 此反应在一定条件下进行2 min后,测得NH3为4 mol。试求:
此反应在一定条件下进行2 min后,测得NH3为4 mol。试求:查看答案和解析>>
科目: 来源:期末题 题型:单选题
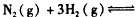
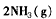 在10 L的密闭容器中进行,测得2 min内,N2的物质的量由20 mol减小到8 mol,则2 min内N2的反应速率为
在10 L的密闭容器中进行,测得2 min内,N2的物质的量由20 mol减小到8 mol,则2 min内N2的反应速率为 查看答案和解析>>
科目: 来源:同步题 题型:单选题
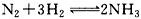 在2s末时,测得容器中含有0.4 mol的NH3,则该反应中H2的化学反应速率是
在2s末时,测得容器中含有0.4 mol的NH3,则该反应中H2的化学反应速率是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com