
科目: 来源:2016-2017学年黑龙江省高一上9月月考化学卷(解析版) 题型:选择题
在标准状况下,将wg A气体(摩尔质量为Mg/mol)溶于1L水中,所得溶液密度为dg/mL,则此溶液的物质的量浓度为( )
A. B.
B.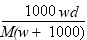 C.
C. D.
D.
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江省高一上9月月考化学卷(解析版) 题型:选择题
分类法是重要的科学研究方法,下列物质归类正确的是( )
A.碱:苛性钠、纯碱、熟石灰
B.盐:胆矾、小苏打、铜绿
C.碱性氧化物:氧化铜、七氧化二锰、氧化铝
D.无丁达尔现象的分散系:碘的四氧化碳溶液、淀粉溶液、氯化铁溶液
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江省高一上9月月考化学卷(解析版) 题型:选择题
若一氧化碳和二氧化碳的混合气体的密度与同温同压下氧气的密度相同,混合气体中一氧化碳和二氧化碳的物质的量之比是( )
A. 1:3 B. 3:1 C. 2:1 D. 1:2
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江省高一上9月月考化学卷(解析版) 题型:选择题
某化学课外小组用海带为原料制取了少量碘水。现用CCl4从碘水中萃取碘并用分液漏斗分离两种溶液。其实验操作可分解为如下几步:
①.把盛有溶液的分液漏斗固定在铁架台上;
②.检验分液漏斗活塞和上口玻璃塞是否漏液;
③.把50 mL碘水和15 mL CCl4加入分液漏斗中,并盖好玻璃塞;
④.压住分液漏斗玻璃塞倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
⑤.从分液漏斗上口倒出上层水溶液;
⑥.放开活塞,用烧杯接收下层溶液;
⑦.将漏斗上口的玻璃塞打开,或使玻璃塞上的凹槽或小孔对准漏斗口上的小孔;
⑧.静置、分层。
A. ②③④①⑧⑦⑤⑥ B. ②③④①⑧⑦⑥⑤
C. ②①③④⑧⑦⑥⑤ D.②③④⑧①⑦⑥⑤
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江省高一上9月月考化学卷(解析版) 题型:选择题
某10% NaOH溶液,加热蒸发掉100g水后得到80mL 20%的溶液,则该20% NaOH溶液的物质的量浓度为( )
A.7 mol/L B.12.5 mol/L C.6.25 mol/L D.7.5 mol/L
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江省高一上9月月考化学卷(解析版) 题型:选择题
同温同压下,等质量的SO2和CO2相比较,下列叙述正确的是( )
A.密度比为16:11 B.分子个数比为16:11
C.体积比为1:1 D.氧原子个数比为1:1
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江省高一上9月月考化学卷(解析版) 题型:选择题
200 mL Fe2(SO4)3溶液中含Fe3+ 56 g,溶液中SO 的物质的量浓度是 ( )
的物质的量浓度是 ( )
A.5 mol/L B. 7.5 mol/L C.10 mol/L D.2.5 mol/L
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江省高一上9月月考化学卷(解析版) 题型:填空题
现有pg某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为___________mol。
(2)该气体所含原子总数为___________个。
(3)该气体在标准状况下的体积为_______________L。
(4)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为__________。
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为________mol·L-1。
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江省高一上9月月考化学卷(解析版) 题型:实验题
现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
甲同学:向1 mol·L-1的氯化铁溶液中加入少量的NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是____________(填“甲”“乙”或“丙”)。
(2)涉及到的化学方程式是________________
(3)证明有Fe(OH)3胶体生成的实验操作是____ ,此现象利用了胶体的一种性质,称为________________。
(4)向制得的Fe(OH)3胶体中加入饱和的硫酸铵溶液,产生的现象是 ,原因是 ;若加入逐滴加入过量稀硫酸,产生的现象
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江省高一上9月月考化学卷(解析版) 题型:实验题
实验室用密度为1.18g/mL,质量分数为36.5%浓盐酸配制250mL0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250mL0.1mol/L的盐酸溶液应量取盐酸体积 mL,所需要的仪器有 .
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1﹣2cm处
(3)容量瓶是配制溶液的必需仪器.下列关于容量瓶及其使用方法的叙述,错误的是 .
①是配制一定物质的量浓度的溶液的专用仪器
②使用前要先检查容量瓶是否漏液
③容量瓶可以用来加热
④不能用容量瓶长期贮存配制好的溶液
⑤可以用500mL容量瓶配制250mL溶液
⑥容量瓶上标有的是温度、容量、刻度线
a.①③ b.①④ c.③⑤ d.⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com