
科目: 来源:2016-2017年黑龙江哈尔滨师大附中高二10月月考化学卷(解析版) 题型:选择题
在一个容积为V L的密闭容器中放入2 mol A(g)和1 mol B(g),在一定条件下发生下列反应3A(g)+ B(g) nC(g)+2D(g) 达到平衡后,A物质的量浓度减小1/2,混合气体的平均摩尔质量增大1/8,则该反应的化学方程式中n的值是
nC(g)+2D(g) 达到平衡后,A物质的量浓度减小1/2,混合气体的平均摩尔质量增大1/8,则该反应的化学方程式中n的值是
A、1 B、2 C、3 D、4
查看答案和解析>>
科目: 来源:2016-2017年黑龙江哈尔滨师大附中高二10月月考化学卷(解析版) 题型:选择题
右图是温度和压强对X+Y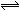 2Z反应影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
2Z反应影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
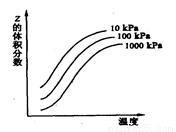
A.上述可逆反应的正反应为放热反应
B.X、Y、Z均为气态
C.X和Y中只有一种为气态,Z为气态
D. 上述反应的逆反应的ΔH>0
查看答案和解析>>
科目: 来源:2016-2017年黑龙江哈尔滨师大附中高二10月月考化学卷(解析版) 题型:选择题
一定条件下,可逆反应的平衡常数可以用平衡浓度计算, 也可以用平衡分压代替平衡浓度计算,分压=总压×物质的量分数。在恒温恒压条件下,总压不变,用平衡分压计算平衡常数更方便。下列说法不正确的是
也可以用平衡分压代替平衡浓度计算,分压=总压×物质的量分数。在恒温恒压条件下,总压不变,用平衡分压计算平衡常数更方便。下列说法不正确的是
A.对于C2H4(g)+H2O(g)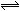 C2H5OH(g)在一定条件下达到平衡状态时,体系的总压强为P,其中C2H4(g)、H2O(g)、C2H5OH(g)均为1 mol,则用分压表示的平衡常数KP=3/P
C2H5OH(g)在一定条件下达到平衡状态时,体系的总压强为P,其中C2H4(g)、H2O(g)、C2H5OH(g)均为1 mol,则用分压表示的平衡常数KP=3/P
B.恒温恒压下,在一容积可变的容器中,反应2A(g)+B(g)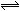 2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、 2 mol和4 mol.若此时A、B和C均增加1 mol,平衡正向移动
2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、 2 mol和4 mol.若此时A、B和C均增加1 mol,平衡正向移动
C.恒温恒压下,在一容积可变的容器中,N2(g)+3H2(g)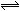 2NH3(g)达到平衡状态时,N2、H2、NH3各1 mol,若此时再充入3 mol N2,则平衡正向移动
2NH3(g)达到平衡状态时,N2、H2、NH3各1 mol,若此时再充入3 mol N2,则平衡正向移动
D.对于一定条件下的某一可逆反应,用平衡浓度表示的平衡常数和用平衡分压表示的平衡常数,其数值不同,但意义相同,都只与温度有关
查看答案和解析>>
科目: 来源:2016-2017年黑龙江哈尔滨师大附中高二10月月考化学卷(解析版) 题型:选择题
在恒温时,一固定压强的容器内发生如下反应:2NO2(g) 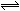 N2O4(g),达平衡时再向容器内通一定量的NO2(g)重达平衡后,与第一次平衡时相比,NO2的体积分数
N2O4(g),达平衡时再向容器内通一定量的NO2(g)重达平衡后,与第一次平衡时相比,NO2的体积分数
A、不变 B、增大 C、减小 D、无法判断
查看答案和解析>>
科目: 来源:2016-2017年黑龙江哈尔滨师大附中高二10月月考化学卷(解析版) 题型:选择题
在密闭容器中发生反应m A(g)+n B(g) 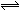 p C(g),达到平衡后,保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.9倍,下列说法正确的是
p C(g),达到平衡后,保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.9倍,下列说法正确的是
A.m+n>p B.平衡向逆反应方向移动 C.A的转化率提高 D.C的体积分数增加
查看答案和解析>>
科目: 来源:2016-2017年黑龙江哈尔滨师大附中高二10月月考化学卷(解析版) 题型:选择题
在容积一定的 密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:C(s)+2NO(g)
密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:C(s)+2NO(g) CO2(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是
CO2(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是
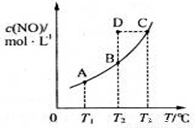
A.该反应的△H>0
B.若该反应在T1、T2时的平衡常数分别为K1、K2 ,则K1<K2
,则K1<K2
C.在T2时,若反应体系处于状态D,则此时v正>v逆
D.若状态B、C、D的压强分别为PB、PC 、PD ,则 PC=PD>PB
查看答案和解析>>
科目: 来源:2016-2017年黑龙江哈尔滨师大附中高二10月月考化学卷(解析版) 题型:填空题
(1)下列物质中,属于弱电解质的是(填序号,下同) ,属于非电解质是 。
①硫酸氢钠固体 ②次氯酸钠 ③氯化氢气体 ④蔗糖 ⑤硫酸钡 ⑥氨气 ⑦冰醋酸
(2)写出下 列物质在水中的电离方程式:碳酸: 。次氯酸钠: 。
列物质在水中的电离方程式:碳酸: 。次氯酸钠: 。
(3)甲、乙两瓶氨水的浓度分别为1 mol•L-1、0.1 mol•L-1,则c(OH﹣)甲:c(OH﹣)乙 10(填“大于”、“等于”或“小于”)。
(4)现有常温条件下甲、乙、丙三种溶液,甲为0.1 mol•L-1的NaOH溶液,乙为0.1 mol• L-1的HCl溶液,丙为0.1 mol•L-1的CH3COOH溶液,甲、乙、丙三种溶液中由水电离出的c(OH﹣)的大小关系为 。
L-1的HCl溶液,丙为0.1 mol•L-1的CH3COOH溶液,甲、乙、丙三种溶液中由水电离出的c(OH﹣)的大小关系为 。
(5)NO2与NO之间存在如下可逆反应:2NO2 2NO+O2。T oC时,在一恒容密闭容器中充入适量NO2,反应达到平衡状态的标志是 。(填序号)
2NO+O2。T oC时,在一恒容密闭容器中充入适量NO2,反应达到平衡状态的标志是 。(填序号)
①混合气体的颜色不再改变的状态
②混合气体的密度不再改变的状态
③混合气体的压强不再改变的状态
④混合气体的平均相对分子质量不再改变的状态
⑤ 的比值不再改变的状态
的比值不再改变的状态
查看答案和解析>>
科目: 来源:2016-2017年黑龙江哈尔滨师大附中高二10月月考化学卷(解析版) 题型:填空题
在恒温容器中加入1 mol N2和3 mol H2,达到平衡时NH3的体积分数为m%。若N2、H2、NH3的起始加入量分别为x mol、y mol、z mol,达到平衡时NH3的体积分数仍为m%。
(1)该容器恒容,则x、 y、z应满足的关系是 。
y、z应满足的关系是 。
(2)该容器恒压,则x、y、z应满足的关系是 。
(3)若该容器恒压,前者达到平衡时生成NH3为a moL,则后者达到平衡时生成NH3 mol(用a、x、z表示)。
查看答案和解析>>
科目: 来源:2016-2017年黑龙江哈尔滨师大附中高二10月月考化学卷(解析版) 题型:实验题
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有________________________。
(2)硫酸铜溶液可以加快氢气生成速率的原因是________________________。
(3)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是________。
(4)要加快上述实验中气体产生的速率,还可采取的措施有____________________(答两种)。
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
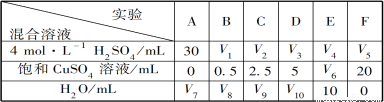
请完成此实验设计,其中:V1=___________,V6=___________,V9=___________;
反应一段时间后,实验A中的金属呈___________色,实验E中的金属呈___________色;
该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因___________。
查看答案和解析>>
科目: 来源:2016-2017年黑龙江哈尔滨师大附中高二10月月考化学卷(解析版) 题型:计算题
将等物质的量A、B混合于2 L的密闭容器中,发生如下反应: ,经5 min后,测得D的浓度为0.5 mol•L-1,
,经5 min后,测得D的浓度为0.5 mol•L-1,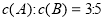 ,
,
C的平均反应速率是0.1 mol•L-1•min-1
求:(1)此时A的浓度及反应 开始前放入容器中A、B物质的量。
开始前放入容器中A、B物质的量。
(2)B的平均反应速率。
(3)x值是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com