
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标准状况) | 2.24L | 3.36L | 3.36L |
| A. | 15.7 g混合物恰好与盐酸完全反应 | |
| B. | NaHCO3占混合物的物质的量分数为50% | |
| C. | 盐酸的物质的量浓度为3.0 mol/L | |
| D. | 加入混合物9.2 g时盐酸过量 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2.3 g Na投入到97.7 g水中形成的溶液溶质质量分数为2.3% | |
| B. | 25 g CuSO4•5H2O溶于75 g水之后,溶质的质量分数为16% | |
| C. | Na2O2溶于水后溶质未发生改变 | |
| D. | 6.2 g Na2O溶于水后溶质仍为6.2 g |
查看答案和解析>>
科目: 来源: 题型:解答题
 ,不考虑立体异构)是临床上使用广泛的药物.下图所示的为其多条合成路线中的一条(反应试剂和反应条件均未标出)
,不考虑立体异构)是临床上使用广泛的药物.下图所示的为其多条合成路线中的一条(反应试剂和反应条件均未标出)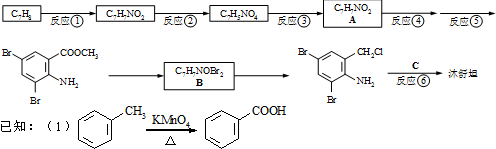
 +2
+2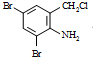 +K2CO3→2
+K2CO3→2 +2KCl+CO2↑+H2O
+2KCl+CO2↑+H2O B
B
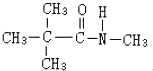 、
、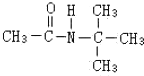
查看答案和解析>>
科目: 来源: 题型:解答题
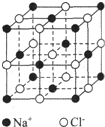
查看答案和解析>>
科目: 来源: 题型:填空题
 目前流行的关于生命起源假设的理论认为,生命起源于约40亿年前的古洋底的热液环境,这种环境系统中普遍存在铁硫簇结构,如Fe2S2、Fe4S4、Fe8S7等,这些铁硫簇结构参与了生命起源的相关反应.某化学兴趣小组在研究某铁硫簇结构的组成时,设计了下列实验.
目前流行的关于生命起源假设的理论认为,生命起源于约40亿年前的古洋底的热液环境,这种环境系统中普遍存在铁硫簇结构,如Fe2S2、Fe4S4、Fe8S7等,这些铁硫簇结构参与了生命起源的相关反应.某化学兴趣小组在研究某铁硫簇结构的组成时,设计了下列实验.| 滴定次数 | 待测溶液体积/mL | 草酸溶液体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.50 | 23.70 |
| 2 | 25.00 | 1.02 | 26.03 |
| 3 | 25.00 | 0.00 | 24.99 |
| 编号 | 温度/℃ | 酸化的H2C2O4溶液/mL | KMnO4溶液/mL | 溶液褪色时间/s |
| 1 | 25 | 5.0 | 2.0 | 40 |
| 2 | 25 | 5.0(另加少量可溶于水的MnSO4粉末) | 2.0 | 4 |
| 3 | 60 | 5.0 | 2.0 | 25 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | PM2.5是指直径为2.5pm颗粒物 | |
| B. | PM2.5造成的雾霾天气,空气质量很差,对人体健康危害极大 | |
| C. | 空气中的PM2.5,表示每立方米空气中直径小于或等于2.5um的颗粒物的含量,则PM2.5可能导致空气形成气溶胶 | |
| D. | 无风雾霾中的PM2.5的运动应属于布朗运动 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 22 mL、12 mL | B. | 13 mL、21 mL | C. | 16 mL、16 mL | D. | 21 mL、13 mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com