
科目: 来源: 题型:解答题
 .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
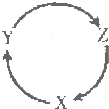 下表各组物质中,满足下图物质一步转化关系的选项是( )
下表各组物质中,满足下图物质一步转化关系的选项是( )| X | Y | Z | |
| A | Na | NaOH | NaHCO3 |
| B | Cu | CuSO4 | Cu(OH)2 |
| C | Cl2 | HCl | NaCl |
| D | Si | SiO2 | H3SiO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向次氯酸钙溶液中通入SO2:Ca2++2ClO-+H2O+SO2═CaSO3↓+2HClO | |
| B. | 硫酸铝钾溶液中滴加氢氧化钡直到沉淀质量最大:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ | |
| C. | 硫氢化钠发生电离:HS-+H2O═H3O++S2- | |
| D. | 用食醋检验牙膏中的摩擦剂碳酸钙:CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子半径由小到大的顺序:X<Y<Z<W | |
| B. | X氢化物的沸点高于Z氢化物的沸点 | |
| C. | 最高价氧化物对应水化物的酸性X大于Z | |
| D. | 室温下,0.1 mol/L W的气态氢化物的水溶液的pH>1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ca2+、K+、Cl-、SO32- | B. | NH4+、Fe2+、I一、SO42- | ||
| C. | Na+、K+、ClO-、S2- | D. | Na+、S2O32-、AlO2-、K+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NA个Fe(OH)3胶体粒子的质量为107g | |
| B. | 8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA | |
| C. | 1 molCl2与足量Fe反应转移电子数一定为2NA | |
| D. | 2.3gNa与氧气完全反应,反应中转移的电子数0.1NA |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com