
科目: 来源: 题型:选择题
| A. | 水分子中共价键比氯化钠中离子键弱 | |
| B. | 水的相对分子质量比氯化钠的小 | |
| C. | 水分子间有范德华力,氯化钠分子间的作用力较强 | |
| D. | 水分子间是以范德华力相结合,相互作用较弱;氯化钠晶体中,Na+和Cl-以离子键相结合,作用力较强 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | c(NH4+):②>④>③>① | B. | pH:②>③>④>① | ||
| C. | c(H+):①>③>②>④ | D. | c(NH3•H2O):②>④>③>① |
查看答案和解析>>
科目: 来源: 题型:选择题
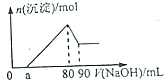 Fe2O3和Al2O3的混合物完全溶解于160mL2mol/LHCl溶液中,在所得溶液中滴加NaOH溶液得到如图,下列说法不正确的是( )
Fe2O3和Al2O3的混合物完全溶解于160mL2mol/LHCl溶液中,在所得溶液中滴加NaOH溶液得到如图,下列说法不正确的是( )| A. | 若a=20mL时,则混合物中Fe2O3占0.02mol | |
| B. | 所滴加的Na0H溶液的浓度为4mol/L | |
| C. | a点处,Na0H溶液的体积为a<50mL | |
| D. | 若a=20mL,则剩余盐酸的体积为20mL |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1L1mol/L的碳酸钠溶液中含CO32-NA个 | |
| B. | 标准状况下,11.2L甲醇与足量钠反应,可生成标准状况下氢气5.6L | |
| C. | H2O2和H2O的混合物1mol中,含阴离子个数为NA | |
| D. | 标准状况下,22.4LCl2与足量铁充分反应,电子转移数为2NA |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
| 装置 | 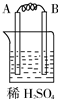 甲 甲 | 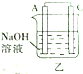 | 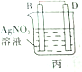 | 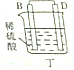 |
| 现象 | A不断溶解 | A极有气泡产生 | B电极质量增加 | B、D电极均无明显变化 |
查看答案和解析>>
科目: 来源: 题型:填空题
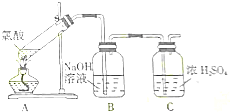
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com