
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 任何化学反应都伴随有能量的变化 | |
| B. | 化学能与电能的相互转化必须通过一定的装置 | |
| C. | 太阳能、风能、氢能、电能都是可再生的新能源 | |
| D. | 能源的开发和利用情况可以衡量一个国家或地区的经济发展和科学技术水平 |
查看答案和解析>>
科目: 来源: 题型:解答题
 B.
B. C.
C. D.
D.
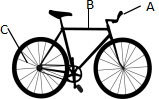
 B.
B.
查看答案和解析>>
科目: 来源: 题型:解答题
| 污 染 指 数 | ||
| SO2 | NO2 | PM10 |
| 49 | 21 | 23 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
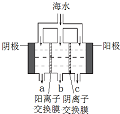 海洋是丰富的资源宝库,通过海水的综合利用可获得许多物质供人类使用.
海洋是丰富的资源宝库,通过海水的综合利用可获得许多物质供人类使用.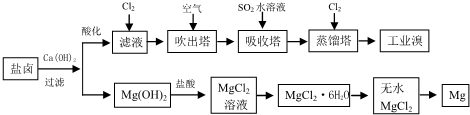
查看答案和解析>>
科目: 来源: 题型:选择题
| A | 乙烷(乙烯) | 溴水 | 分液 |
| B | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| C | 乙醇(少量水) | CaO | 蒸馏 |
| D | 乙醇(苯酚) | 适量的溴水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.2 mol/L | B. | 0.01 mol/L | C. | 0.1 mol/L | D. | 0.02 mol/L |
查看答案和解析>>
科目: 来源: 题型:填空题
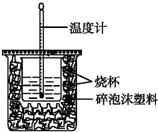 (1)已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1.用50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
(1)已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1.用50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com