
科目: 来源: 题型:选择题
| A. | SiO2既能与HF反应,又能与NaOH反应,属于两性氧化物 | |
| B. | 玛瑙和红宝石的主要成分都是SiO2,SiO2和Si都是制造半导体的材料 | |
| C. | 高温下SiO2能与Na2CO3反应放出CO2,说明H2SiO3的酸性强于H2CO3 | |
| D. | Na2SiO3溶液中加入盐酸可制备硅酸胶体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氧化还原反应中得失电子总数一定相等 | |
| B. | 有单质参加的反应一定是氧化还原反应 | |
| C. | 电解质溶液中阴阳离子的总数一定相等 | |
| D. | 分解反应一定是氧化还原反应 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NH4HCO3溶液与过量KOH溶液反应的离子方程式:NH4++HCO3-+2OH-═NH3•H2O+CO32-+H2O | |
| B. | 向Ba(OH)2溶液中滴入少量KHSO4溶液的离子方程式:SO42-+H++Ba2++OH-═BaSO4↓+H2O | |
| C. | 明矾水解的离子方程式:Al3++3H2O?Al(OH)3+3H+ | |
| D. | K37ClO3与浓盐酸(HCl)在加热时生成氯气的化学方程式:K37ClO3+6HCl═K37Cl+3Cl2↑+3H2O |
查看答案和解析>>
科目: 来源: 题型:解答题
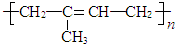 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | C2H5OH+CH3COOH$→_{△}^{浓硫酸}$CH3COOC2H5+H2O | |
| B. | H-C≡C-H+HCl$\stackrel{催化剂}{→}$H2C=CHCl | |
| C. | 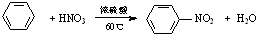 | |
| D. |  |
查看答案和解析>>
科目: 来源: 题型:解答题
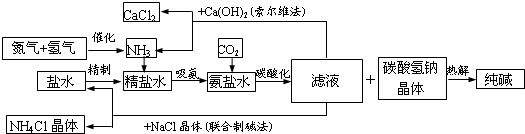
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | X与Z均只能形成一种氧化物 | |
| B. | 离子半径r(Y)<r(Z) | |
| C. | W的最高价氧化物对应的水化物是强酸 | |
| D. | Y的气态氢化物的热稳定性比W的弱 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Al2O3→NaAlO2 | B. | Fe→FeCl3 | C. | Na2O→Na2CO3 | D. | SiO2→H2SiO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com