
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 加入催化剂会改变反应的焓变 | |
| B. | 已知2C(s)+2O2(g)═2CO2(g)△H1,2C(s)+O2(g)═2CO(g)△H2,则△H1<△H2 | |
| C. | 含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(aq);△H=-57.4 kJ/mol | |
| D. | 已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 离子半径:A2->D->B+ | |
| B. | 元素B、C的最高价氧化物对应水化物的碱性:B>C | |
| C. | 简单氢化物的稳定性:A>D | |
| D. | A与B形成的化合物中可能既有离子键又有共价键 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 7.8g苯中含有的碳碳双键数目为0.3NA | |
| B. | 标准状况下,22.4L Cl2通入足量的石灰乳制备漂白粉,转移电子数为2NA | |
| C. | 常温常压下,17g甲基(-14CH3)中所含的中子数为9NA | |
| D. | 4.6g金属钠与足量O2充分反应后,所得固体中阴、阳离子的总数为0.3NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 | |
| A | Fe3+、I-、ClO- | NaOH溶液 | Fe3++3OH-═Fe(OH)3↓ |
| B | Fe2+、NO3-、K+ | 稀硫酸 | 3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O |
| C | Ba2+、HCO3-、Cl- | NaOH溶液 | HCO3-+OH-═CO32-+H2O |
| D | Ag+、F-、NO3- | 过量氨水 | Ag++OH-═AgOH↓ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题
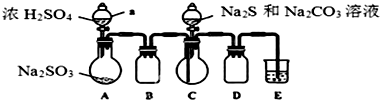
| 实验步骤 | 预期现象或结论 |
| 步骤1:取少量固体样品溶于无氧蒸馏水中 | 固体完全溶解得无色澄清溶液 |
| 步骤2:加入过量盐酸 | |
| 步骤3:静置后取上清液,加入BaCl2溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①中的I2为固态,②中的I2为气态 | |
| B. | ②的反应物总能量比①的反应物总能量低 | |
| C. | ①的产物比②的产物热稳定性更好 | |
| D. | 1 mol固态碘升华时将吸热17 kJ |
查看答案和解析>>
科目: 来源: 题型:选择题
| 序号 | ① | ② | ③ | ④ |
| 溶液 | CH3COONa | NaHCO3 | Na2CO3 | NaClO |
| pH | 8.8 | 9.7 | 11.6 | 10.3 |
| A. | 将等浓度的CH3COOH和HClO溶液,pH小的是HClO | |
| B. | Na2CO3和NaHCO3溶液中粒子种类不同 | |
| C. | 溶液水的电离程度①>②>④>③ | |
| D. | NaHCO3溶液中,c(Na +)=c(CO3 2-)+c(HCO3-)+c(H2CO3) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com