
科目: 来源: 题型:选择题
| A. | 难溶于水的BaCO3是弱电解质 | |
| B. | 0.1mol/L的CH3COOH溶液中H+浓度为0.1mol/L | |
| C. | 强电解质水溶液的导电能力一定比弱电解质的强 | |
| D. | 电解质溶液导电的原因是溶液中有自由移动的阴、阳离子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 胶体是纯净物 | |
| B. | 胶体与溶液的本质区别是有丁达尔效应 | |
| C. | Al(OH)3胶体具有很强的吸附能力,能凝聚水中的悬浮物,也能吸附色素,可做净水剂 | |
| D. | 胶体粒子可以透过半透膜 |
查看答案和解析>>
科目: 来源: 题型:解答题
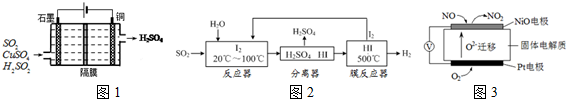
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1.8g水所含有的电子数目为NA | |
| B. | 等物质的量的CaCO3和KHCO3的质量均为100g | |
| C. | 11.2L氧气所含分子数目为0.5NA | |
| D. | 200mL 0.5mol/L Na2SO4溶液所含Na+数目0.1NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用惰性电极电解某溶液时,若两极分别只有H2和O2生成,电解一段时间后,该溶液的浓度可能减小 | |
| B. | 电解精炼铜时,电解质溶液中铜离子浓度不变 | |
| C. | 纯锌与稀硫酸反应时,加入少量CuSO4溶液,可使反应速率加快 | |
| D. | 要使电解后的CuSO4溶液复原,可向其中加人Cu(OH)2固体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 被氧化和被还原的元素分别为铜和氮 | |
| B. | 当产生0.2mol气体时,转移电子为0.6mol | |
| C. | 被还原的CuO占参与反应CuO的$\frac{1}{2}$ | |
| D. | 参加反应的氧化剂和还原剂的物质的量之比为3:2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | SO2使溴水和品红溶液褪色,体现了SO2的漂白性 | |
| B. | 氨气的水溶液能导电,说明氨气是电解质 | |
| C. | 单质硅化学性质稳定,但自然界不存在游离态的硅 | |
| D. | 镁、铝、铜等金属一般采用热还原法冶炼 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 4g D2和足量O2反应可生成D2O的分子数目为2NA | |
| B. | 0.1molCl2与足量NaOH溶液反应,转移电子的数目为0.2NA | |
| C. | 在标准状况下,2.24L氨气所含的电子总数为NA | |
| D. | 标准状况下,6.4 g氧气和臭氧中含有的分子总数为0.2 NA |
查看答案和解析>>
科目: 来源: 题型:解答题
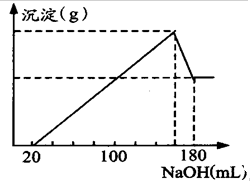 将一定质量的镁、铝合金投入100mL一定物质的量浓度HCl中,合金全部溶解,向所得溶液中滴加5mol/LNaOH溶液到过量,
将一定质量的镁、铝合金投入100mL一定物质的量浓度HCl中,合金全部溶解,向所得溶液中滴加5mol/LNaOH溶液到过量,查看答案和解析>>
科目: 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com