
科目: 来源: 题型:选择题
| A. | 平衡向正反应方向移动了 | B. | 物质A的转化率增加了 | ||
| C. | 物质B的质量分数减少了 | D. | b>a |
查看答案和解析>>
科目: 来源: 题型:解答题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.1 | 8.8 | 11.6 | 10.3 | 11.1 | 11.3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | “忽闻海上有仙山,山在虚无缥缈间”的海市蜃楼是一种自然现象,与胶体知识有关 | |
| B. | “水乳交融,火上浇油”前者包含物理变化,而后者包含化学变化 | |
| C. | “滴水石穿、绳锯木断”不包含化学变化 | |
| D. | “落汤螃蟹着红袍”肯定发生了化学变化 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
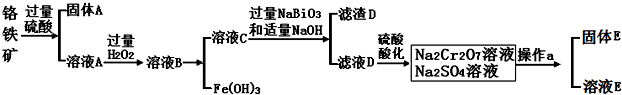
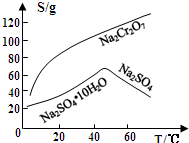

查看答案和解析>>
科目: 来源: 题型:选择题
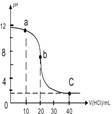
| A. | a点时,溶液呈碱性,溶液中c(B+)>c(Cl-) | |
| B. | b点时溶液的pH=7 | |
| C. | 当c(B+)=c(Cl-)时,v(HCl)<20mL | |
| D. | c点时溶液的c(H+)约为0.03mol•L-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将移液管里下端残液吹入锥形瓶 | |
| B. | 滴定时向锥形瓶中加入少量的蒸馏水后继续滴定 | |
| C. | 滴定管用蒸馏水洗涤后未用标准碱液润洗就装入标准碱液进行滴定 | |
| D. | 用酚酞作指示剂 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 盐酸的物质的量浓度是0.5mol•L-1 | B. | 氢氧化钠溶液的体积是250mL | ||
| C. | 铁和硅的物质的量之比为2:1 | D. | 铁和硅的质量之比为1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com