
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:解答题
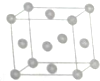 A、B、C、D、M为原子序数依次增大的五种元素,A是元素周期表中原子半径最小的元素;B的一种单质在自然界中硬度最大;C、D的单质都是空气的主要成分;M位于元素周期表的第四周期第6纵行.
A、B、C、D、M为原子序数依次增大的五种元素,A是元素周期表中原子半径最小的元素;B的一种单质在自然界中硬度最大;C、D的单质都是空气的主要成分;M位于元素周期表的第四周期第6纵行.查看答案和解析>>
科目: 来源: 题型:填空题
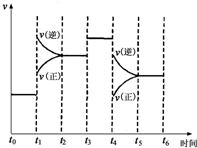 如图表示反应N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ/mol.在某段时间t0~t6中反应速率与反应过程的曲线图
如图表示反应N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ/mol.在某段时间t0~t6中反应速率与反应过程的曲线图查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na与H2O 的反应是熵增的放热反应,该反应能自发进行 | |
| B. | 相同条件下,等质量的碳按a、b两种途径完全转化,途径途径a比途径b放出更多热能途径途径a:C $→_{高温}^{H_{2}O}$CO+H2 $→_{燃烧}^{O_{2}}$CO2+H2O 途径b:C$→_{燃烧}^{O_{2}}$ CO2 | |
| C. | FeCl3和MnO2均可 加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同 | |
| D. | Mg在CO2中燃烧生成MgO和C的反应中,化学能全部转化为热能 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 表示碳原子,用
表示碳原子,用  表示氧原子,用
表示氧原子,用  表示氮原子,如图为气体转换的微观过程.请你根据图示回答下列问题:
表示氮原子,如图为气体转换的微观过程.请你根据图示回答下列问题: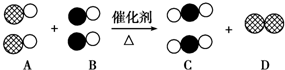
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com