
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 可以电解熔融的氯化钠来制取金属钠 | |
| B. | 可以将钠加入氯化镁饱和溶液中制取镁 | |
| C. | 用电解法冶炼铝时,原料是氯化铝 | |
| D. | 在浓缩的海水加入新制氯水即可得到液溴 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 依图象可知反应:CO(g)+H2O(g)?CO2(g)+H2(g) | |
| B. | 无法判断反应物总能量与生成物总能量的相对大小 | |
| C. | 表示此反应是吸热反应 | |
| D. | 此反应:△H>0 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | S原子的电子层数比Cl原子的电子层数多 | |
| B. | Cl的氢化物的沸点比S的氢化物沸点低 | |
| C. | Cl的气态氢化物比S的气态氢化物稳定 | |
| D. | Cl的失电子能力比S强 |
查看答案和解析>>
科目: 来源: 题型:选择题
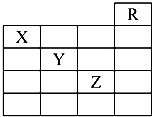 如图是元素周期表的一部分,关于元素X、Y、Z的叙述中,正确的个数是( )
如图是元素周期表的一部分,关于元素X、Y、Z的叙述中,正确的个数是( )| A. | 4个 | B. | 3个 | C. | 2个 | D. | 1个 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 单质的颜色逐渐加深 | B. | 单质的熔沸点逐渐降低 | ||
| C. | 单质的密度逐渐减小 | D. | 单质在水中的溶解度逐渐增大 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 碱金属单质的密度都比水小 | |
| B. | 碱金属单质都是还原剂 | |
| C. | 碱金属单质的熔沸点一般随着原子的电子层数的增多而升高 | |
| D. | 碱金属单质在氧气中燃烧,产物都是过氧化物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ②⑤ | D. | ⑤ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 都属于氧化还原反应 | B. | 发生还原反应的元素相同 | ||
| C. | 发生氧化反应的元素不同 | D. | 生成KCl的物质的量为2:1 |
查看答案和解析>>
科目: 来源: 题型:填空题
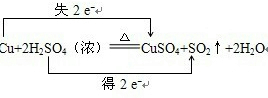 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com