
科目: 来源: 题型:解答题
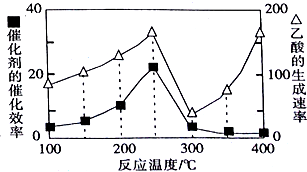
| 物质 | H2 | CO | CH4 | CH3COOH |
| 燃烧热(kJ/mol) | 286 | 283 | 890 | 874 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A | BaCl2与Na2SO4溶液 | Ba(OH)2与H2SO4溶液 |
| B | 石灰石与硝酸反应 | 生石灰与盐酸 |
| C | 氢氧化钠与盐酸 | 氢氧化钠与硫酸氢钠 |
| D | Na2CO3溶液与硝酸溶液 | CaCO3与硝酸溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,将m1克锌加入到m2克20%的盐酸中放出nLH2,则转移电子数为$\frac{n{N}_{A}}{11.2}$ | |
| B. | 0.1mol/L的100mL H2SO3溶液中,含有的离子数约为0.03NA | |
| C. | 9gD2O中含有的电子数为5NA | |
| D. | 120g由NaHSO4和KHSO3组成的混合物中共含有3NA的阴阳离子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ag+>Cu2+>Fe2+ | B. | Cu2+>Ag+>Fe2+ | C. | Ag+>Fe2+>Cu2+ | D. | Fe2+>Cu2+>Ag+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ②不对 | B. | ③④不对 | C. | ①④不对 | D. | 全部正确 |
查看答案和解析>>
科目: 来源: 题型:解答题
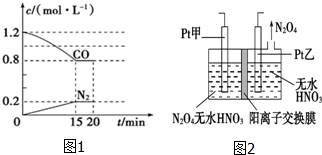 “霾”是当今世界环境热点话题.目前我国许多地方空气质量恶化原因之一是机动车尾气和燃煤产生的烟气.NO和CO气体均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:
“霾”是当今世界环境热点话题.目前我国许多地方空气质量恶化原因之一是机动车尾气和燃煤产生的烟气.NO和CO气体均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 铝在空气中耐腐蚀,所以铝是不活泼金属 | |
| B. | 铝能与冷水反应 | |
| C. | 铝热反应常用于冶炼某些熔点较高的金属 | |
| D. | 冶炼铝可用电解AlCl3的方法 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③④⑤ | B. | ①③⑤ | C. | ①②⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 升高温度 | B. | 降低温度 | C. | 通入氦气 | D. | 加入催化剂 | ||||
| E. | 移出氧气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com