
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 增大B的浓度,v(正)>v(逆) | |
| B. | 升高温度,平衡向逆反应方向移动,v(正)减小 | |
| C. | 压强增大一倍,平衡不移动,v (正)、v(逆)不变 | |
| D. | 增加A的量,平衡向正反应方向移动 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 中性溶液的AG=1 | |
| B. | 常温下0.1 mol•L-1NaOH溶液的AG=12 | |
| C. | 酸性溶液的AG<0 | |
| D. | 常温下0.1 mol•L-1盐酸溶液的AG=12 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | X、Y、Z的分子个数比为3:1:2 | |
| B. | X的生成速率与Z的生成速率相等 | |
| C. | 混合气体的密度不再改变 | |
| D. | 单位时间内生成3n mol X,同时消耗n mol Y |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 葡萄糖、蔗糖均能水解 | |
| B. | 福尔马林、水玻璃、一水合氨均为混合物 | |
| C. | 反应:NH4Cl (s)═NH3(g)+HCl(g)在室温下不能自发进行,说明该反应的△H>0 | |
| D. | C(石墨,s)═C (金刚石,s)△H=+1.9kJ•mol-1,说明金刚石比石墨稳定 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 都正确 | B. | ②③④⑤ | C. | ②③⑤ | D. | ②④⑤ |
查看答案和解析>>
科目: 来源: 题型:选择题
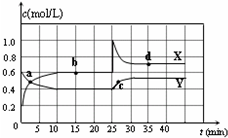 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )| A. | 图中Y曲线是表示NO2浓度随时间的变化曲线 | |
| B. | 前10 min内v(N2O4)为0.1 mol/( L•min) | |
| C. | 25 min时,导致平衡移动的原因是将密闭容器的体积缩小为1L | |
| D. | 25 min时,导致平衡移动的原因是向容器通入适量NO2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 水的电离程度始终增大 | |
| B. | 当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO?) | |
| C. | c(CH3COOH)与c(CH3COO?)之和始终保持不变 | |
| D. | $\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O}$先增大再减小 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com