
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 25℃时,将0.02 mol•L-1的氨水与a mol•L-1的盐酸等体积混合(体积变化忽略不计),反应后溶液呈中性,则用含a的代数式表示NH3•H2O的电离常数为Kb=$\frac{a×1{0}^{-7}}{0.02-a}$ | |
| B. | 往银氨溶液中加水稀释,反应②平衡向逆反应方向移动 | |
| C. | 若往银氨溶液中加入足量的盐酸,则溶液中会产生白色浑浊 | |
| D. | 已知:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则1 L 0.1 mol•L-1氨水和足量的盐酸反应放出的热量等于5.73 kJ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将等体积的①、②溶液混合后,盐酸会抑制醋酸的电离,所以pH>2 | |
| B. | 将一定体积的②、③溶液混合后,溶液显碱性,则该混合溶液中c(Cl-)>c(NH4+) | |
| C. | 将一定体积的①、④溶液混合后,溶液显酸性,则V(NaOH)可能等于V(CH3COOH) | |
| D. | 向等体积的③、④溶液中加水稀释10倍,稀释后溶液中由水电离的c(H+):③>④ |
查看答案和解析>>
科目: 来源: 题型:选择题
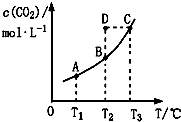
| A. | 该反应的△H<0 | |
| B. | 在T2时,D点的反应速率:ν(正)<(逆) | |
| C. | A、C两点相比,混合气体的平均相对分子质量:M(A)<M(C) | |
| D. | 若T1、T2时的平衡常数分别为K1、K2,则K1>K2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 10℃20mL 3 mol•L-1的NaHCO3溶液 | B. | 20℃30mL 2 mol•L-1的NaHCO3溶液 | ||
| C. | 20℃10mL 4 mol•L-1的NaHCO3溶液 | D. | 10℃10mL 2 mol•L-1的NaHCO3溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 加水稀释后,溶液中c(H+)减小 | |
| B. | 加入少量NaOH固体,电离度增大,溶液的pH增大 | |
| C. | 加入少量NH4Cl固体,氨水电离平衡向右移动 | |
| D. | 通入少量HCl气体后,电离平衡常数不变 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 与铝反应产生H2的溶液中:Na+、K+、S2-、CO32- | |
| B. | 加入酚酞显红色的溶液中:K+、Na+、Cl-、CH3COO- | |
| C. | pH=2的溶液中:NH4+、Na+、Fe2+、NO3-、Cl- | |
| D. | 由水电离出的c(H+)=1×10-12mol•L-1的溶液中:K+、Na+、Cl-、Al3+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 新制的氯水在光照下颜色逐渐变浅 | |
| B. | H2、I2、HI平衡混合气缩小体积加压后颜色变深 | |
| C. | 工业上生产硫酸的过程中,SO2在催化氧化时条件控制为常压,而不是高压 | |
| D. | 工业上合成氨气时温度选择450℃左右,而不是常温 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下,0.1 mol•L-1 CH3COOH溶液的pH=3 | |
| B. | CH3COOH溶液能和NaOH溶液反应 | |
| C. | 往CH3COOH溶液中加入几滴石蕊试液,溶液变红色 | |
| D. | 0.1 mol•L-1CH3COOH溶液做导电性实验,灯光较暗 |
查看答案和解析>>
科目: 来源: 题型:选择题
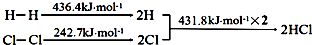
| A. | H-H键比Cl-Cl键稳定 | |
| B. | △H=-184.5 kJ•mol-1 | |
| C. | 正反应活化能比逆反应活化能高 | |
| D. | 在相同条件下,1mol H2(g)和1mol Cl2(g)分别在点燃和光照条件下反应生成2mol HCl(g),重新恢复到原来的状态时△H相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com