
科目: 来源:同步题 题型:不定项选择题
| 将质量分数为0.052(5.2%)的NaOH溶液1 L(密度为1.06 g·cm-3)用铂电极电解,当溶液中NaOH的质量分数改变了0.010(1.0%)时停止电解,则此时溶液中应符合的关系是 | ||||||||||||||||||||
|
[ ] | ||||||||||||||||||||
|
查看答案和解析>>
科目: 来源:0103 月考题 题型:单选题
[ ]
查看答案和解析>>
科目: 来源:福建省模拟题 题型:单选题
查看答案和解析>>
科目: 来源:期末题 题型:填空题
在50mL 0.2mol·L-1硫酸铜溶液中插入两个电极,通电电解(不考虑水分蒸发),则:
(1)若两极均为铜片,试说明电解过程中浓度将怎样变化_________________。
(2)若阳极为纯锌,阴极为铜片,阳极反应式是____________________。
(3)如不考虑H+在阴极上放电,当电路中有0.04mol电子通过时,阴极增重___________g,阴极上的电极反应式是_______________。
查看答案和解析>>
科目: 来源:同步题 题型:不定项选择题
 NaOH+H2↑+Cl2↑。
NaOH+H2↑+Cl2↑。查看答案和解析>>
科目: 来源:0101 期中题 题型:不定项选择题
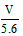 mol
mol 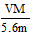
 mol
mol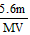
查看答案和解析>>
科目: 来源:模拟题 题型:单选题
查看答案和解析>>
科目: 来源:0115 模拟题 题型:填空题

 CH3OH(g);CO的转化率(α)与温度、压强的关系如下图所示。
CH3OH(g);CO的转化率(α)与温度、压强的关系如下图所示。 
查看答案和解析>>
科目: 来源:0108 月考题 题型:单选题
[ ]
查看答案和解析>>
科目: 来源:同步题 题型:不定项选择题
[ ]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com