
科目: 来源: 题型:解答题
| 温度/K | 反应Ⅰ | 反应Ⅱ | 已知: K1>K2>K1′>K2′ |
| 298 | K1 | K2 | |
| 328 | K1′ | K2′ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaH+H2O═NaOH+H2↑ | B. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ | ||
| C. | F2+H2O═2HF+O2↑ | D. | Cl2+H2O?HCl+HClO |
查看答案和解析>>
科目: 来源: 题型:解答题
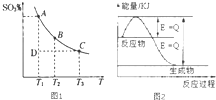 运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.查看答案和解析>>
科目: 来源: 题型:选择题
 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成化学式为Z2T的离子化合物.五种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成化学式为Z2T的离子化合物.五种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )| A. | 原子半径和离子半径均满足:Y<Z | |
| B. | 最高价氧化物对应的水化物的酸性:T<R | |
| C. | 气态氢化物的稳定性:Y>T | |
| D. | 由X、Y、Z、T四种元素组成的化合物水溶液一定呈中性 |
查看答案和解析>>
科目: 来源: 题型:选择题
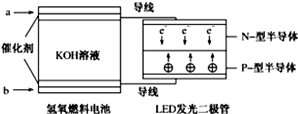 下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )
下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )| A. | 氢氧燃料电池中OH-向b极移动 | |
| B. | 该装置中只涉及两种形式的能量转化 | |
| C. | H2在负极发生氧化反应 | |
| D. | P一型半导体连接电池负极 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 硫酸与水 | B. | 氯化钠与水 | C. | 熟石灰与水 | D. | 生石灰与水 |
查看答案和解析>>
科目: 来源: 题型:选择题
 )是生产汽油清洁剂的中间产物.下列关于聚异丁烯的说法中错误的是( )
)是生产汽油清洁剂的中间产物.下列关于聚异丁烯的说法中错误的是( )| A. | 聚异丁烯可以通过加聚反应制得 | |
| B. | 聚异丁烯的分子式为(C4H8)n | |
| C. | 聚异丁烯能使溴的四氯化碳溶液褪色 | |
| D. | 聚异丁烯完全燃烧生成CO2 和H2O的物质的量相等 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 纤维素$\stackrel{水解}{→}$葡萄糖$\stackrel{氧化}{→}$CO2和H2O(释放能量维持生命活动) | |
| B. | 淀粉$\stackrel{水解}{→}$葡萄糖$\stackrel{氧化}{→}$CO2和H2O(释放能量维持生命活动) | |
| C. | 蛋白质$\stackrel{水解}{→}$氨基酸$\stackrel{合成}{→}$人体所需的蛋白质(人体生长发育) | |
| D. | 油脂$\stackrel{水解}{→}$甘油和高级脂肪酸$\stackrel{氧化}{→}$CO2和H2O(释放能量维持生命活动) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1.0 mol | B. | 2.0 mol | C. | 3.0 mol | D. | 4.0 mol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na与水反应时增大水的用量 | |
| B. | Fe与稀硫酸反应制取H2 时,改用浓硫酸 | |
| C. | 在K2SO4与BaCl2两溶液反应时,降低温度 | |
| D. | Al与氧气燃烧生成Al2O3,将Al片改为Al粉, |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com