
科目: 来源: 题型:解答题
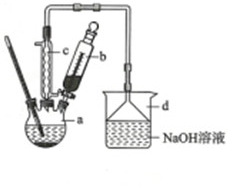
| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
科目: 来源: 题型:解答题

| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |

查看答案和解析>>
科目: 来源: 题型:填空题
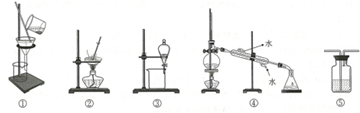
 利用下列各组中的物质制备并收集少量相应的气体,能采用如图装置的是(2)(3)(9)
利用下列各组中的物质制备并收集少量相应的气体,能采用如图装置的是(2)(3)(9)查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 制乙烯:浓硫酸、乙醇,用酒精灯迅速加热至170℃ | |
| B. | 制硝基苯:浓硝酸、浓硫酸、苯,用55~60℃水浴加热 | |
| C. | 制乙酸乙酯:乙醇、浓硫酸、冰醋酸,用酒精灯缓慢加热 | |
| D. | 制酚醛树脂:苯酚、40%的甲醛溶液、浓盐酸,用沸水浴加热 |
查看答案和解析>>
科目: 来源: 题型:多选题

| A. | 甲:醋酸;乙:纯碱;丙:苯酚钠溶液 证明酸性:CH3COOH>H2CO3>C6H5OH | |
| B. | 甲:10%过氧化氢溶液;乙:二氧化锰;丙:硫酸酸化的KI溶液 证明氧化性:O2>I2 | |
| C. | 甲:浓盐酸;乙:KMnO4 丙:KBr溶液 证明氧化性:KMnO4>Cl2>Br2 | |
| D. | 甲:饱和食盐水;乙:电石;丙:溴水 证明稳定性:H2O>C2H2>Br2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 蒸馏法是用海水制备淡水的主要方法之一 | |
| B. | 将饱和FeCl3溶液滴入到沸腾的蒸馏水中制备Fe(OH)3胶体 | |
| C. | 将氯气通入到热的氢氧化钠浓溶液中制备漂白液 | |
| D. | 用油脂的碱性水解反应制取肥皂 |
查看答案和解析>>
科目: 来源: 题型:解答题
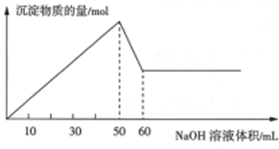
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com