
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
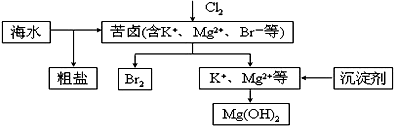 氯气在实验室和生产中都有重要的应用.
氯气在实验室和生产中都有重要的应用.查看答案和解析>>
科目: 来源: 题型:解答题
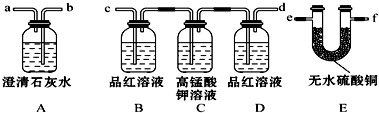

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 一定不存在的离子是Mg2+、Ba2+,不能确定是否含有K+、NO3- | |
| B. | 一定存在的离子是CO32-、SO42-,CO32-的物质的量浓度为0.25mol•L-1,SO42-的物质的量浓度为0.1mol•L-1 | |
| C. | 一定存在的离子是CO32-、SO42-、K+,其中K+浓度≥0.2mol•L-1 | |
| D. | 一定存在的离子是CO32-、SO42-、K+,其中K+浓度为0.2mol•L-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2.7g | B. | 8.1g | C. | 5.4g | D. | 10.8g |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氨气可以用浓硫酸干燥也可用碱石灰干燥 | |
| B. | 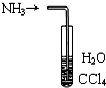 用如图装置吸收NH3可防止倒吸 用如图装置吸收NH3可防止倒吸 | |
| C. | 氨水能导电,所以NH3是电解质 | |
| D. | 氨气可以使湿润的蓝色石蕊试纸变红,依此可检验氨气 |
查看答案和解析>>
科目: 来源: 题型:解答题
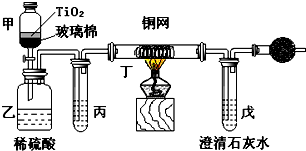 电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol•L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞.
电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol•L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+)=7:2时,2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O | |
| B. | CuCl2溶液与NaHS溶液反应,当n(CuCl2):n(NaHS)=1:2时Cu2++2HS-═CuS↓+H2S↑ | |
| C. | Cl2与FeBr2溶液反应,当n(Cl2):n(FeBr2)=1:1时,2Fe2++4Br-+3Cl2═2 Fe3++2Br2+6Cl- | |
| D. | Fe与稀硝酸反应,当n(Fe):n(HNO3)=3:8时,3Fe+2NO3-+8H+═3Fe2++2NO↑+4H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com