
科目: 来源: 题型:选择题
| A. | 等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-═Mg(OH)2↓ | |
| B. | 向Fe(NO3)3溶液中通入足量HI气体:2Fe3++2I-═2Fe2++I2 | |
| C. | 向NaHCO3溶液中滴入少量澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| D. | 向水玻璃溶液中通入过量CO2:SiO32-+H2O+CO2═CO32-+H2SiO3↓ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | KClO3 | B. | KMnO4 | C. | MnO2 | D. | Ca(ClO)2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.1 mol•L-1的H2SO4溶液中含有H+的数目为0.2NA | |
| B. | 过氧化钠与水反应时,生成0.1molO2转移电子0.2NA | |
| C. | 1.0L 1.0mol•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| D. | 3.36LCO2和O2的混合气体所含的氧原子数目为0.3NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | 将铜粉加入1.0mol/LFe2(SO4)3溶液中 | 溶液变蓝,有黑色固体出现 | 金属铁比铜活泼 |
| C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| D | 在相同条件下,分别加热Na2CO3固体和NaHCO3固体 | NaHCO3固体分解,产生气体使澄清石灰水变浑浊,Na2CO3固体并没有分解 | Na2CO3固体的稳定性比NaHCO3好 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 金属钠着火时使用泡沫灭火器灭火 | |
| B. | 用试管加热碳酸氢钠固体时使试管竖直向上 | |
| C. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 | |
| D. | 进行石油分馏操作时,加入碎瓷片 |
查看答案和解析>>
科目: 来源: 题型:解答题
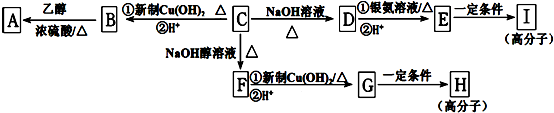
 ;
;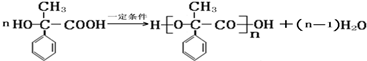 ,该反应类型是缩聚反应;
,该反应类型是缩聚反应; ,该反应类型是加聚反应;
,该反应类型是加聚反应; .
.查看答案和解析>>
科目: 来源: 题型:解答题
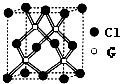 A、B、C、D、E、F、G为原子序数依次增大的前四周期元素.A、F原子的最外层电子数均等于其周期序数.F原子的电子层数是A的3倍; B原子核外电子分处3个不同能级.且每个能级上排布的电子数相同;A与C形成的最简单分子为三角锥形;D原子p轨道上成对电子数等于未成对电子数;E原子核外每个原子轨道上的电子都已成对.E与F同周期;G的原子序数等于A、C、D、F 四种元素原子序数之和.
A、B、C、D、E、F、G为原子序数依次增大的前四周期元素.A、F原子的最外层电子数均等于其周期序数.F原子的电子层数是A的3倍; B原子核外电子分处3个不同能级.且每个能级上排布的电子数相同;A与C形成的最简单分子为三角锥形;D原子p轨道上成对电子数等于未成对电子数;E原子核外每个原子轨道上的电子都已成对.E与F同周期;G的原子序数等于A、C、D、F 四种元素原子序数之和. ;回答E与F原子的第一电离能的大小关系怎样,原因是Mg原子3s能级为全满稳定结构,能量较低;
;回答E与F原子的第一电离能的大小关系怎样,原因是Mg原子3s能级为全满稳定结构,能量较低;查看答案和解析>>
科目: 来源: 题型:解答题
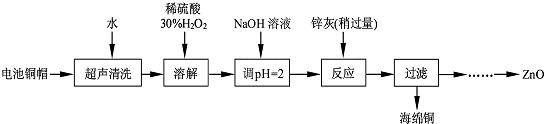
| 实验编号 | 1 | 2 | 3 | 4 |
| V(Na2S2O3)(mL) | 28.32 | 25.31 | 25.30 | 25.32 |
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
查看答案和解析>>
科目: 来源: 题型:解答题
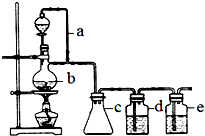 某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙酸乙酯(乙酸):加饱和Na2CO3溶液,充分振荡静置后,分液,弃水层 | |
| B. | 苯(苯酚):加溴水,振荡,过滤除去沉淀 | |
| C. | 溴乙烷(乙醇):多次加水振荡,分液,弃水层 | |
| D. | 乙醇(水):加入新制生石灰,蒸馏,收集馏出物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com