
科目: 来源: 题型:选择题
| 化学式 | 电离常数(25℃) |
| CH3COOH | K1=1.7×10-5 |
| HClO | K1=3.0×10-8 |
| H2CO3 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | 如表提供的数据下:HClO、HCO3-、ClO-、CO32- | |
| B. | pH=3的溶液中:CO32-、Na+、SO42-、AlO2- | |
| C. | 能与Al反应生成H2的溶液:NH4+、Ca2+、NO3-、I- | |
| D. | c(H+)=1×10-14mol/L的溶液:K+、Na+、AlO2-、S2O32- |
查看答案和解析>>
科目: 来源: 题型:多选题
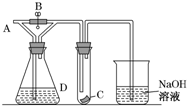 如图所示,A处通入干燥Cl2,关闭B阀时,C处的红色布条看不到明显现象,打开B阀后,C处红色布条逐渐褪色,则D瓶中装的是( )
如图所示,A处通入干燥Cl2,关闭B阀时,C处的红色布条看不到明显现象,打开B阀后,C处红色布条逐渐褪色,则D瓶中装的是( )| A. | 浓H2SO4 | B. | NaOH溶液 | C. | 浓盐酸 | D. | 饱和NaCl溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②③⑤ | B. | ③④⑥⑦ | C. | ①③④⑥ | D. | ②③⑥⑦ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目: 来源: 题型:解答题
| 酸或碱 | 电离平衡常数(Ka或Kb) |
| CH3COOH | 1.8×10-5 |
| HNO2 | 4.6×10-4 |
| HCN | 5×10-10 |
| HClO | 3×10-8 |
| NH3•H2O | 1.8×10-5 |
| 难(微)溶物 | 溶度积常数(Ksp) |
| BaSO4 | 1×10-10 |
| BaCO3 | 2.6×10-9 |
| CaSO4 | 7×10-5 |
| CaCO3 | 5×10-9 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 苯环上有两个取代基的C9H12,其苯环上一氯代物的同分异构体(不考虑立体异构)共有10种 | |
| B. | 某只含有C、H、O、N的有机物的简易球棍模型如图所示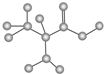 ,该有机物与CH3CH2CH2NO2互为同系物 ,该有机物与CH3CH2CH2NO2互为同系物 | |
| C. | 2,2-二甲基丙醇与 2-甲基丁醇互为同分异构体 | |
| D. | S诱抗素的分子结构如右图所示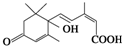 ,则该分子的分子式为C15H20O4 ,则该分子的分子式为C15H20O4 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
| 电解质 | Ka1 | Ka2 |
| H2S | 1.3×10-7 | 7.1×10-15 |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | K+、Fe2+、NO3-、Cl- | B. | Na+、SO42-、Ba2+、H+ | ||
| C. | Na+、CO32-、Cl-、NO3- | D. | Al3+、K+、Cl-、SO42- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 被还原的物质是氧化剂 | |
| B. | 还原剂被还原、氧化剂被氧化 | |
| C. | 得电子、化合价升高的物质是氧化剂 | |
| D. | 氧化剂反应后得到氧化产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com