
科目: 来源: 题型:选择题
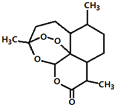 我国科学家屠呦呦获2015年诺贝尔生理学或医学奖.她研究得到的青蒿素挽救了数百万疟疾病人的生命,有关青蒿素说法不合理的是( )
我国科学家屠呦呦获2015年诺贝尔生理学或医学奖.她研究得到的青蒿素挽救了数百万疟疾病人的生命,有关青蒿素说法不合理的是( )| A. | 化学式为C15H22O5 | |
| B. | 能发生取代反应和氧化反应 | |
| C. | 在H2SO4或 NaOH溶液中均不能稳定存在 | |
| D. | 可用乙醇从青蒿浸取液中萃取出青蒿素 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 点燃铝粉可以引发NH4ClO4分解 | |
| B. | NH4ClO4迅速分解时可能会引发爆炸 | |
| C. | NH4ClO4应低温通风保存,远离火种、热源 | |
| D. | 0.5 mol NH4ClO4分解时产生的气体体积是44.8 L |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H2CO3的电离方程式为 H2CO3═H++HCO3- | |
| B. | 向AgCl的饱和溶液中加入足量浓AgNO3溶液,溶液中各离子浓度不变 | |
| C. | 常温下,PH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序:c(Cl-)>c(NH4+)>c(H+)=C(OH-) | |
| D. | NH4+的水解反应离子方程式:NH4++H2O?NH3•H2O+H+ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
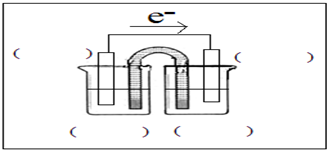 能量之间可以相互转化:原电池可将化学能转化为电能.
能量之间可以相互转化:原电池可将化学能转化为电能.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com