
科目: 来源: 题型:多选题
| A. | 硫酸 | B. | 氢硫酸 | C. | 硝酸 | D. | 碘化钾 |
查看答案和解析>>
科目: 来源: 题型:解答题
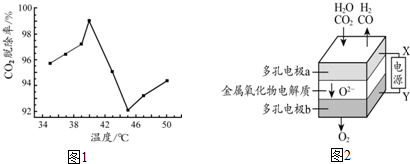
查看答案和解析>>
科目: 来源: 题型:解答题
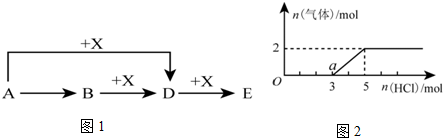
查看答案和解析>>
科目: 来源: 题型:选择题
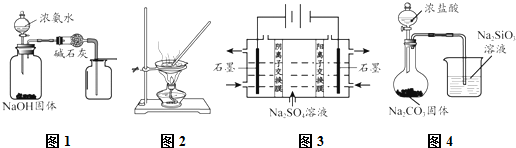
| A. | 用图1所示装置制取并收集干燥纯净的NH3 | |
| B. | 用图2所示装置蒸发FeCl3溶液制备无水FeCl3 | |
| C. | 用图3所示装置制硫酸和氢氧化钠 | |
| D. | 用图4所示装置比较HCl、H2CO3和H2SiO3的酸性强弱 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 根据以上信息,可推断NH3•H2O为弱电解质 | |
| B. | 加水稀释过程中,c(H+)•c(OH-) 的值增大 | |
| C. | 加入K2CO3固体可促进 NH4+的水解 | |
| D. | 同pH的NH4Cl溶液和CH3COOH溶液,由水电离出的c(H+) 前者大 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 共价键 | H-H | Cl-Cl | H-Cl |
| E (kJ •mol-1) | 436 | 243 | 432 |
| A. | H2(g)+Cl2(g)=2HCl (g)△H=+247 kJ•mol-1 | |
| B. | H (g)+Cl (g)→HCl (g)△△H=+432 kJ•mol-1 | |
| C. | 1 mol H2(g) 与1 mol Cl2(g) 的总能量高于2 mol HCl (g) 的总能量 | |
| D. | 用电子式表示HCl的形成过程 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaCN中碳元素化合价为+2价 | |
| B. | NaCN中含有离子键和极性共价键 | |
| C. | H2O2既做氧化剂又做还原剂 | |
| D. | 当有0.1 mol NH3生成时,有0.2 mol电子转移 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1 mol Na2O2固体中含离子总数为4 NA | |
| B. | 标准状况下,22.4 L N2和H2混合气中含NA个原子 | |
| C. | 常温下,pH=13的NaOH溶液中OH-离子数目为0.1 NA | |
| D. | 3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol,若反应放出9.2 kJ热量,则参加反应的氢分子数目为0.3 NA |
查看答案和解析>>
科目: 来源: 题型:选择题
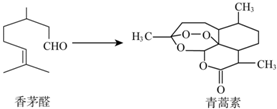
| A. | 香茅醛能使Br2的CCl4溶液褪色 | |
| B. | 青蒿素分子式为C15H22O5 | |
| C. | 青蒿素在一定条件下可发生水解反应 | |
| D. | 二者均可与氢气发生加成反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 明矾做净水剂:Al3++3H2O═Al (OH)3↓+3H+ | |
| B. | 小苏打治疗胃酸过多:CO32-+2H+═CO2↑+H2O | |
| C. | 漂白液加白醋,提高漂白效率:CH3COOH+ClO-═HClO+CH3COO- | |
| D. | 酸化的淀粉碘化钾溶液在空气中放置一段时间变蓝:4I-+O2+2H2O═2I2+4OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com