
科目: 来源: 题型:选择题
| A. | 稳定性:HI<HBr<HCl<HF | B. | 元素非金属性:Si<P<S<Cl | ||
| C. | 沸点:正丁烷>异丁烷>丙烷 | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 一定是甲烷与乙烷的混合物 | B. | 可能是甲烷与丙烷的混合物 | ||
| C. | 一定含有乙烷 | D. | 可能是甲烷与己烷的混合物 |
查看答案和解析>>
科目: 来源: 题型:解答题

 .
.查看答案和解析>>
科目: 来源: 题型:解答题

| 氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |

查看答案和解析>>
科目: 来源: 题型:解答题
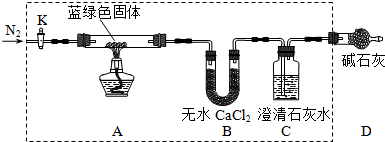
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 溶解度(25℃):小苏打<苏打 | B. | 沸点:H2Se>H2S>H2O | ||
| C. | 密度:溴乙烷>水 | D. | 碳碳键键长:乙烯<苯 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 4.6g乙醇与足量的钠反应放出1.12L氢气 | |
| B. | 可用苯或大豆油从溴水中萃取溴 | |
| C. | 0.1mol丙烷中含有约6.02×1023个共价键 | |
| D. | 分子式为C4H9Cl的有机物共有5种 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NO2与于恒容容器中生成1molN2O4 | B. | NO2与于恒压容器中生成1molN2O4 | ||
| C. | N2O4与于恒容容器中生成1molNO2 | D. | N2O4与于恒压容器中生成1molNO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com