
科目: 来源: 题型:填空题
 2Ag(NH3)2+(aq)+2OH-(aq)△H=(2a-b)kJ?mol-1;
2Ag(NH3)2+(aq)+2OH-(aq)△H=(2a-b)kJ?mol-1;查看答案和解析>>
科目: 来源: 题型:选择题
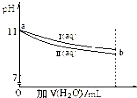
| A. | I 和 II 溶液中,离子种类数相同 | |
| B. | a 点处,I 溶液的浓度为 10-3mol?L-1 | |
| C. | a 点处,I、II 对水的电离平衡影响相同 | |
| D. | b 处的 I、II 溶液分别与盐酸反应,I 消耗 HCl 物质的量比 II 多 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 实验 | 实验目的 |
| A.测定等物质的量浓度的 CH3COONa和Na2S溶液pH | 比较 CH3COOH和H2S的酸性强弱 |
B.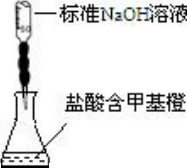 | 测定盐酸的浓度 |
C.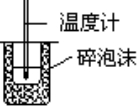 | 测定中和热 |
| D.先用酚酞,后用甲基橙作指示剂,用标准盐酸滴定0.1 mol/L的Na2CO3溶液 | 证明 CO32-水解分两步 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | n1>n2 | B. | n1=n2 | C. | n2>n1 | D. | c(F-)<c(CN-) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 白醋中滴入石蕊试液呈红色 | B. | 白醋加入豆浆中有沉淀产生 | ||
| C. | pH 试纸显示白醋的 pH 为 2~3 | D. | 蛋壳浸泡在白醋中有气体放出 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氯水能导电,所以氯气是电解质 | |
| B. | CaCO3不溶于水,所以它是非电解质 | |
| C. | NaHCO3是强电解质,所以它的水溶液中不存在电离平衡 | |
| D. | 体积相同,c(OH-)相同的氨水和 NaOH 溶液被中和,前者消耗 HCl 多,所以NH3•H2O 是弱电解质 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | BaSO4(s)?Ba2+(aq)+SO42-(aq) | B. | HClO=H++ClO- | ||
| C. | NaHSO3=Na++H++SO32- | D. | H2S+H2O?H3O++HS- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在氮化铝的合成反应中,N2是还原剂,Al2O3氧化剂 | |
| B. | 氮化铝是铝合金中的一种 | |
| C. | 上述反应中每生成2molAlN,N失去6mol电子 | |
| D. | 氮化铝中氮元素的化合价为-3 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
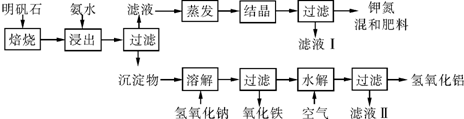
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com