
科目: 来源: 题型:选择题
| A. | 少量的钠保存在煤油中 | |
| B. | 铁粉要密封保存并置于干燥处 | |
| C. | 浓盐酸保存在密封玻璃瓶中 | |
| D. | 氢氧化钠溶液保存在玻璃塞的玻璃瓶中 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 生铁是混合物,钢是纯净物 | |
| B. | 用铁矿石来炼铁时,要加入如焦炭等氧化剂 | |
| C. | 不锈钢是铁和硅的合金,比纯铁硬度大,不易腐蚀 | |
| D. | 钢比生铁含碳量低 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 开发新能源,如太阳能、风能等,减少对化石能源的依赖,也减少对大气的污染 | |
| B. | 直径接近于2.5×10-6m的颗粒物(PM2.5)分散在空气中形成的混合物具有丁达尔效应 | |
| C. | 实施“煤改气”、“煤改电”等清洁燃料改造工程,有利于保护环境 | |
| D. | 汽油发动机工作时会产生一定量的NO和CO,采用三元催化装置可以减少污染物的排放 |
查看答案和解析>>
科目: 来源: 题型:解答题
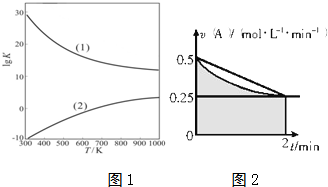
查看答案和解析>>
科目: 来源: 题型:解答题
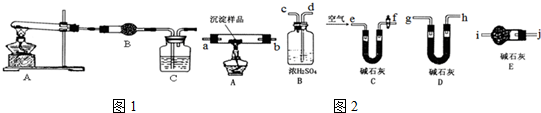
查看答案和解析>>
科目: 来源: 题型:解答题
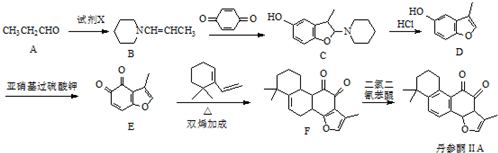
 .
.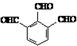 .
.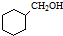 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.查看答案和解析>>
科目: 来源: 题型:解答题
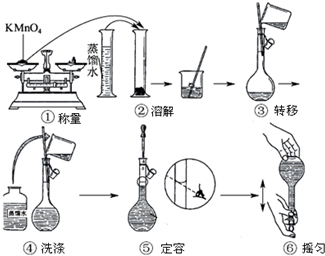
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 浓硝酸和浓硫酸都具有很强的腐蚀性、脱水性 | |
| B. | 冷的浓硫酸和浓硝酸都可以用铝、铁的容器盛装 | |
| C. | 稀硫酸和稀硝酸都具有氧化性 | |
| D. | 硫酸和硝酸都是重要的化工原料 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 碳酸钙与硝酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 铁与稀硫酸反应:Fe+2H+═Fe2++H2↑ | |
| C. | 将氨气通入盐酸中:NH3+HCl═NH4++Cl- | |
| D. | 氢氧化钡溶液中滴加稀硫酸:OH-+H+═H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com