
科目: 来源: 题型:选择题
| A. | 二者在一定的条件下可以相互转化 | |
| B. | 二者热稳定性不同,碳酸钠的热稳定性大于碳酸氢钠的热稳定性 | |
| C. | 等质量的碳酸钠与碳酸氢钠与足量盐酸反应,后者现象更剧烈,但前者产生的二氧化碳多 | |
| D. | 将二氧化碳通入到饱和碳酸钠溶液中,会有浑浊产生 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向淀粉碘化钾溶液中加入氯水,溶液变为蓝色,可证明Cl2的氧化性强于I2 | |
| B. | 向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- | |
| C. | 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ | |
| D. | 氯水能使有色花瓣褪色,说明氯水中含有Cl2 |
查看答案和解析>>
科目: 来源: 题型:解答题
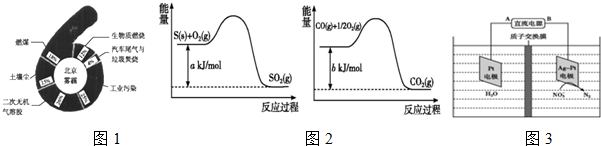
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | c(Na+)=c(HA-)+2c(A2-)+c(OH-) | |
| B. | c(H2A)+c(HA-)+c(A2-)=0.1 mol•L-1 | |
| C. | 将上述溶液稀释至0.01 mol•L-1,c(H+)•c(OH-)不变 | |
| D. | 溶液中存在:c(Na+)>c(HA-)>c(OH-)>c(H2A)>c(H+)>c( A2-) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.1 mol•L-1的NaHCO3溶液中:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) | |
| B. | 等物质的量浓度的三种溶液:①(NH4)2SO4、②NH4Cl、③NH3•H2O中,c(NH4+)的大小顺序为:③>②>① | |
| C. | 25℃时,pH=4的KHC2O4溶液中:c(HC2O4-)>c(H2C2O4)>c(C2O22-) | |
| D. | CH3COONa溶液和盐酸混合呈中性的溶液中:c(Na+)>c(Cl-)=c(CH3COOH) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na+的结构示意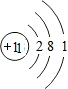 | |
| B. | CO2的结构式:O-C-O | |
| C. | CH4分子的比例模型为: | |
| D. | 用电子式表示氯化氢分子的形成过程:H•+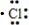 →H+[ →H+[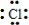 ]- ]- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,11.2L甲醛气体中电子数为8NA | |
| B. | 25℃时,pH=12的NaCN溶液中水电离的H+数为10-12NA | |
| C. | 1L0.5mol•L-1的CHCOOH溶液中所含的离子数和分子总数为0.5NA | |
| D. | 10mol•L-1100mL的浓硝酸与足量铜反应,硝酸得到的电子数为0.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com