
科目: 来源: 题型:选择题
| A. | X、Z两种元素可形成X2Z和X2Y2两种常见共价化合物 | |
| B. | 工业上常用电解熔融的W和M氯化物的方法分别制取W、M两种单质 | |
| C. | M的最高价氧化物与Y、W两元素最高价氧化物对应水化物均能反应生成盐和水 | |
| D. | X与W可形成离子化合物,且该离子化合物具有较强还原性 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 溶质的质量分数为ω=$\frac{a}{{V}_{ρ}-a}$×100% | |
| B. | 溶质的物质的量浓度c=$\frac{1000a}{17V}$mol•L-1 | |
| C. | 溶液中c(OH-)=$\frac{1000b}{V}$mol•L-1+c(H+) | |
| D. | 上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HCl | B. | FeCl2 | C. | KOH | D. | Na2CO3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用广泛pH试纸测得某溶液的pH为3.5 | |
| B. | 用25mL量筒量取12.36mL盐酸 | |
| C. | 用托盘天平称量8.7g食盐 | |
| D. | 将40 g NaOH溶解于1 L 水中配得1 mol•L-1的溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na+、H+、NO3-、CO32- | B. | Na+、Fe3+、Cl-、SCN- | ||
| C. | K+、Cu2+、SO42-、OH- | D. | Na+、Al3+、NO3-、Cl- |
查看答案和解析>>
科目: 来源: 题型:解答题
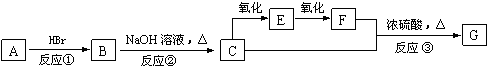
查看答案和解析>>
科目: 来源: 题型:解答题
 如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物,已知:
如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物,已知:查看答案和解析>>
科目: 来源: 题型:填空题
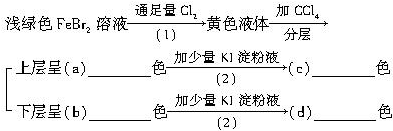
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com