
科目: 来源: 题型:选择题
| A. | AgNO3 | B. | HCl | C. | BaCl2 | D. | NaOH |
查看答案和解析>>
科目: 来源: 题型:解答题
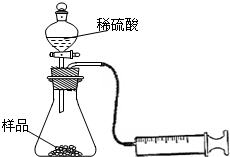 某学校化学科研小组从文献资料上获得如下信息:NaHCO3在潮湿的空气中会缓慢分解成Na2CO3、H2O和CO2.为了验证这一信息,该科研小组将一瓶在潮湿空气中久置的NaHCO3样品混合均匀后,进行如下实验:
某学校化学科研小组从文献资料上获得如下信息:NaHCO3在潮湿的空气中会缓慢分解成Na2CO3、H2O和CO2.为了验证这一信息,该科研小组将一瓶在潮湿空气中久置的NaHCO3样品混合均匀后,进行如下实验:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ba(OH)2 | B. | NaOH | C. | BaCl2 | D. | AgNO3 |
查看答案和解析>>
科目: 来源: 题型:解答题
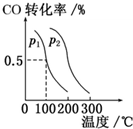 联合国气候变化大会于2009年12月7~18日在哥本哈根召开.中国政府承诺到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.
联合国气候变化大会于2009年12月7~18日在哥本哈根召开.中国政府承诺到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H2S与SO2、NO与O2、NH3与HCl在常温下均不能大量共存 | |
| B. | (NH4)2SO3、Ca(ClO)2、NaAlO2均既能和稀硫酸又能和氢氧化钠溶液反应 | |
| C. | Fe(OH)3、FeCl2、FeCl3、NO均可通过化合反应得到 | |
| D. | AlCl3、Fe3O4、NaOH都可通过置换反应一步得到也可通过化合反应一步得到 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ③②①④ | B. | ②③①④ | C. | ③①②④ | D. | ①②③④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氢氟酸易与SiO2反应,可用于刻蚀玻璃 | |
| B. | Al和Fe2O3能发生铝热反应,可用于焊接钢轨 | |
| C. | NH3具有碱性,可用NH3与灼热的CuO作用制取少量N2 | |
| D. | Fe具有良好的导电性,可用Fe作电解食盐水的阴极材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com