
科目: 来源: 题型:选择题
| A. | C2H4、C2H2、CO2 | B. | CH4、CHCl3、CO2 | C. | Cl2、H2、N2 | D. | NH3、H2O、CO2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子半径X>Y>Z | |
| B. | 电负性按X、Y、Z的顺序由弱到强 | |
| C. | 非金属性X>Y>Z | |
| D. | 气态氢化物的稳定性按X、Y、Z的顺序由弱到强 |
查看答案和解析>>
科目: 来源: 题型:填空题
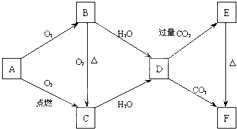 如图所示,A、B、C、D、E、F为金属钠或钠的化合物.
如图所示,A、B、C、D、E、F为金属钠或钠的化合物.查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 分别将它们配制成溶液,再加入澄清石灰水,观察是否有沉淀产生 | |
| B. | 分别将它们配制成溶液,再进行焰色反应,观察火焰颜色 | |
| C. | 分别将它们配制成溶液,再加入BaCl2溶液,观察是否有沉淀产生 | |
| D. | 分别加热,再用澄清石灰水检验是否有气体产生 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 钠与氧气反应的产物与反应条件无关 | |
| B. | 钠在反应中易失电子,表现出还原性 | |
| C. | 钠在氯气中燃烧产生红色火焰 | |
| D. | 钠只有在加热条件下才能与氯气发生反应 |
查看答案和解析>>
科目: 来源: 题型:填空题
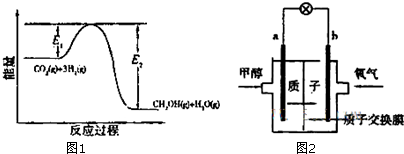
查看答案和解析>>
科目: 来源: 题型:填空题
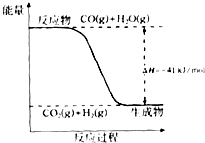 已知一氧化碳与水蒸气反应过程的能量变化如图所示:
已知一氧化碳与水蒸气反应过程的能量变化如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com