
科目: 来源: 题型:选择题
| A. | 二氧化氮与氧气 | B. | 硝酸与水 | ||
| C. | 硝酸与一氧化氮 | D. | 一氧化氮与二氧化氮 |
查看答案和解析>>
科目: 来源: 题型:多选题
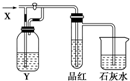 如图:是一套检验气体性质的实验装置.向装置中缓慢通入气体X,若关闭活塞,则品红溶液无变化而澄清的石灰水变浑浊;若打开活塞,则品红溶液褪色.据此判断气体X和洗气瓶内溶液Y分别可能为( )
如图:是一套检验气体性质的实验装置.向装置中缓慢通入气体X,若关闭活塞,则品红溶液无变化而澄清的石灰水变浑浊;若打开活塞,则品红溶液褪色.据此判断气体X和洗气瓶内溶液Y分别可能为( )| A | B | C | D | |
| X | SO2 | SO2 | CO2 | Cl2 |
| Y | 饱和的NaHCO3溶液 | 浓硫酸 | Na2SO3 溶液 | Na2CO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ②⑥ | B. | ②⑤ | C. | ①②⑤⑥ | D. | ②③④⑤ |
查看答案和解析>>
科目: 来源: 题型:解答题
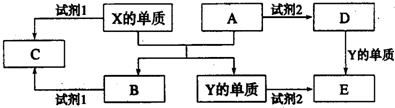
查看答案和解析>>
科目: 来源: 题型:选择题
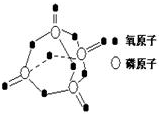 研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1mol化学键时所需吸收的能量.下表是部分化学键的键能数据:
研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1mol化学键时所需吸收的能量.下表是部分化学键的键能数据:| 化学键 | P-P | P-O | O=O | P=O |
| 键能/kJ•mol-1 | 197 | 360 | 499 | X |
| A. | 1057.5 kJ•mol-1 | B. | 335.25 kJ•mol-1 | C. | 433.75 kJ•mol-1 | D. | 959.0 kJ•mol-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | pH=3的硝酸和pH=11的氨水 | B. | pH=3的盐酸和pH=11的氨水 | ||
| C. | pH=3的硫酸和pH=11的KOH | D. | pH=3的醋酸和pH=11的KOH溶液 |
查看答案和解析>>
科目: 来源: 题型:解答题

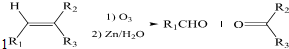

 +HNO3$→_{△}^{浓硫酸}$
+HNO3$→_{△}^{浓硫酸}$ +H2O.
+H2O. .
. (写出其中一种的结构简式).
(写出其中一种的结构简式).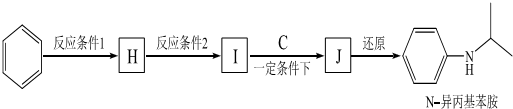
 .
.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com