
科目: 来源: 题型:选择题
| A. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| B. | 用澄清石灰水鉴别SO2 和CO2 | |
| C. | 将Fe(NO3)2 溶于稀盐酸,滴加KSCN 溶液没有颜色变化 | |
| D. | 透闪石的化学成分为Ca2Mg5Si8O22(OH)2 写成氧化物的形式为:2CaO•5MgO•8SiO2•H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
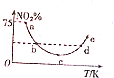 取5等份(各1mol)NO2,分别加入温度不同的2L恒容密闭容器中,发生反应:2NO2(g)?N2O4(g)△H<0.反应10s时,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图,据图分析,下列说法正确的是( )
取5等份(各1mol)NO2,分别加入温度不同的2L恒容密闭容器中,发生反应:2NO2(g)?N2O4(g)△H<0.反应10s时,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图,据图分析,下列说法正确的是( )| A. | 10s内,图中a点对应的N2O4反应速率为0.01mol•L-1•s-1 | |
| B. | 图中b、d两点对应的NO2速率相等 | |
| C. | c点前后平衡移动的方向相反 | |
| D. | e点对应的容器中气体颜色最深 |
查看答案和解析>>
科目: 来源: 题型:选择题
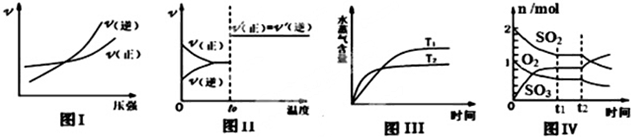
| A. | 图 I:反应 N2+3H 2?2NH3在恒温情况下,反应速率与压强的关系 | |
| B. | 图Ⅱ:反应 H2+I2?2HI 达平衡后,升高温度时反应速率随时间的变化 | |
| C. | 图 III:反应 CO2(g)+H2(g)?CO(g)+H2O(g)△H>0,水蒸气含量随时间的变化 | |
| D. | 图 IV:反应 2SO2+O2?2SO3 达平衡后,缩小容器体积,各成分物质的量随时间的变化 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | ①②④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在某溶液中滴加AgNO3溶液,若产生白色沉淀,说明该溶液中有Cl- | |
| B. | 在某溶液中先滴加盐酸,再滴加AgNO3溶液,若产生白色沉淀,说明溶液中有Cl- | |
| C. | 在某溶液中先滴加AgNO3溶液,产生色沉淀,再滴加盐酸,沉淀不消失,说明溶液中Cl- | |
| D. | 某溶中滴加用HNO3酸化的AgNO3溶液,若产生白色沉淀,说明溶液中有Cl- |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 4、5 | B. | 5、4 | C. | 3、4 | D. | 5、7 |
查看答案和解析>>
科目: 来源: 题型:解答题
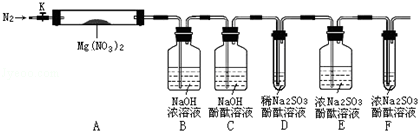
 ,步骤Ⅱ中,通入一段时间N2的目的是避免对分解产物O2的检验产生干扰.
,步骤Ⅱ中,通入一段时间N2的目的是避免对分解产物O2的检验产生干扰.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HF、HCl、HBr、HI的熔点沸点依次升高 | |
| B. | HF、HCl、HBr、HI水溶液的酸性依次升高 | |
| C. | 乙醇易溶于水,是因为乙醇分子与水分子之间只存在范德华力 | |
| D. | 氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com