
科目: 来源: 题型:选择题
| A. | 无色溶液:K+、Cu2+、NO3-、AlO2- | |
| B. | 空气:CH4、CO2、SO2、NO | |
| C. | 氢氧化铁胶体:H+、K+、S2-、Br - | |
| D. | 各离子物质的量浓度相等的溶液:K+、Mg2+、SO42-、NO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 除①外其它都可以 | B. | 只有②③⑤ | C. | 只有①④⑤ | D. | 全部 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 溶液是电中性的,胶体是带电的 | |
| B. | 胶体粒子可以通过半透膜而溶液不行,故可以用半透膜来分离胶体和溶液 | |
| C. | 一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有 | |
| D. | 溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | SiO2溶于水生成的H2SiO3的酸性弱于H2CO3 | |
| B. | SiO2是一种空间立体网状结构的晶体,熔点高、硬度大 | |
| C. | 在SiO2晶体中,每个硅原子周围结合2个氧原子 | |
| D. | SiO2是一种酸性氧化物,所以不和任何酸反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
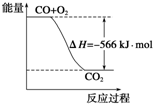 已知:2CO(g)+O2(g)=2CO2(g)△H=-566kJ•mol-1
已知:2CO(g)+O2(g)=2CO2(g)△H=-566kJ•mol-1| A. | CO的燃烧热为283 kJ | |
| B. | 如图可表示由CO生成CO2的反应过程和能量关系 | |
| C. | 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)△H>-532 kJ•mol-1 | |
| D. | CO(g)与Na2O2(s)反应放出549 kJ热量时,电子转移数为6.02×1023 |
查看答案和解析>>
科目: 来源: 题型:解答题
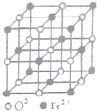 (1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、
(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、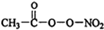 (PAN)等二次污染物.
(PAN)等二次污染物.查看答案和解析>>
科目: 来源: 题型:选择题
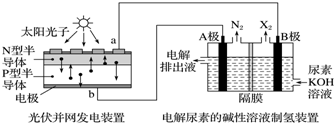
| A. | 工作时,A极的电极上CO(NH2)2放电生成N2反应为还原反应 | |
| B. | 工作时,B极的电极反应式为2H2O+2e-═2OH-+H2↑ | |
| C. | N型半导体为正极,P型半导体为负极 | |
| D. | 制氢装置溶液中电子流向:从B极流向A极 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该溶液中:2c (H+)=c(A-)+c(OH-) | |
| B. | 由pH=3的HA溶液与pH=11的NaOH溶液等体积混合,所得溶液中:c(Na+)>c(A-)>c(OH-)>c(H+) | |
| C. | 浓度均为0.1 mol•L-1的HA和NaA溶液等体积混合,所得溶液中:c(A-)>c(HA)>c(Na+)>c(OH-)>c(H+) | |
| D. | 0.1 mol•L-1 HA溶液与0.05 mol•L-1 NaOH溶液等体积混合,所得溶液中:2c(H+)+c(HA)═c(A-)+2c(OH-) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该电池负极的电极反应为:Al-3e-═Al3+ | |
| B. | 该电池可能是一种可充电的二次电池 | |
| C. | 消耗相同质量金属时,用锂作负极产生电子的物质的量比用铝时多 | |
| D. | 电池工作时,溶液中铝离子向正极移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com