
科目: 来源: 题型:解答题
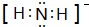 .
.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 该浓硝酸中HNO3的物质的量浓度是12.0 mol/L | |
| B. | 该合金中铜与镁的物质的量之比是2:1 | |
| C. | NO2和N2O4的混合气体中,N2O4的体积分数是20% | |
| D. | 得到2.54g沉淀时,加入NaOH溶液的体积是6.0 mL |
查看答案和解析>>
科目: 来源: 题型:多选题
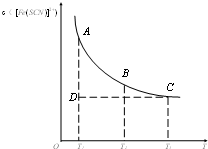 FeCl3(aq)与KSCN(aq)混合时平衡:Fe3+(aq)+SCN-(aq)?Fe(SCN)2+(aq);已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T三关系如图所示,则下列说法正确的是( )
FeCl3(aq)与KSCN(aq)混合时平衡:Fe3+(aq)+SCN-(aq)?Fe(SCN)2+(aq);已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T三关系如图所示,则下列说法正确的是( )| A. | FeCl3(aq)与KSCN(aq)反应是放热反应 | |
| B. | 温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1<K2 | |
| C. | 反应处于D点时,一定有V正>V逆 | |
| D. | A点与B点相比,A点的c(Fe3+)大 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 25℃,0.1mol/L pH=4.5 的NaHC2O4溶液 c(HC2O4-)>c(C2O42-)>c(H2C2O4) | |
| B. | 向0.2mol/L的NaHCO3溶液中加入等体积的0.1mol/L的NaOH溶液c(H+)+c(Na+)=c(OH-)+c(CO32-)+c(HCO3-) | |
| C. | 常温下,氯化铵和氨水的混合溶液其pH=7,c(Cl-)=0.1mol/L c(Cl-)>c(NH4+)>c(OH-)=c(H+) | |
| D. | 浓度均为0.1mol/L的醋酸钠和醋酸的混合溶液中c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 通入足量的二氧化碳后的溶液中Na+、$Al{O_2}^-、$$CH_3^{\;}CO{O^-}、$$C{O_3}^{2-}$ | |
| B. | 无色溶液中$M{g^{2+}}、Mn{O_4}^-、S{O_4}^{2-}、{I^-}$ | |
| C. | 酸性溶液中可能大量存在 $N{a^+}、Cl{O^-}、S{O_4}^{2-}、{I^-}$ | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中$N{H_4}^+、C{l^-}$、Al3+、$N{O_3}^-$ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | $\frac{22.4b}{5a}$ | B. | $\frac{5a}{11.2b}$ | C. | $\frac{22.4a}{5b}$ | D. | $\frac{11.2b}{5a}$ |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 纯净物 | 酸性氧化物 | 碱性氧化物 | 酸 | 盐 |
| A | 碱石灰 | 二氧化硫 | 氧化铝 | 乙二酸 | 小苏打 |
| B | 五水硫酸铜 | 三氧化硫 | 氧化铜 | 油酸 | 苏打 |
| C | 过氧化氢 | 五氧化二磷 | 过氧化物 | 硬脂酸 | 碱式碳酸铜 |
| D | 盐酸 | 一氧化碳 | 氧化镁 | 冰醋酸 | 小苏打 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 主要是用来吸收或滴加少量试剂,以及吸取上层清液,分离沉淀 | |
| B. | 进行滴加的时候,胶头滴管要保持垂直在容器正上方 | |
| C. | 取液体时,先将胶头滴管伸入试剂瓶中,用手指捏紧滴管的胶头再放开手指 | |
| D. | 专用的胶头滴管在使用完之后,就一定要放回原试剂中 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | AlON和石英的化学键类型相同 | B. | 电解熔融AlON可得到Al | ||
| C. | AlON的N元素化合价为-1 | D. | AlON和石英晶体类型相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com