
科目: 来源: 题型:选择题
| A. | 配制240mL溶液需要用到250mL容量瓶 | |
| B. | 用四氯化碳萃取碘水中的碘 | |
| C. | 用过滤的方法分离胶体和溶液 | |
| D. | 蒸馏时应将温度计水银球放在与蒸馏烧瓶的支管口相平处 |
查看答案和解析>>
科目: 来源: 题型:解答题
 CO和H2作为重要的燃料和化工原料,有着十分广泛的应用.
CO和H2作为重要的燃料和化工原料,有着十分广泛的应用.查看答案和解析>>
科目: 来源: 题型:解答题
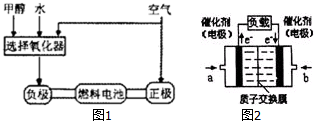
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HCN易溶于水 | |
| B. | 1mol/L氢氰酸溶液的pH约为3 | |
| C. | 10mL1mol/LHCN恰好与10mL1mol/LNaOH溶液完全反应 | |
| D. | HCN溶液的导电性比盐酸溶液的弱 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
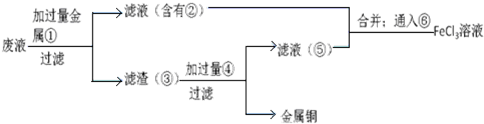
查看答案和解析>>
科目: 来源: 题型:解答题
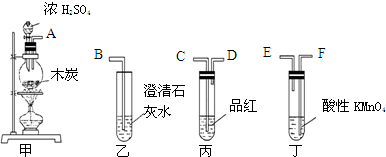
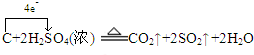 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com