
科目: 来源: 题型:选择题
 我国自主研发制造的国产大型客机C919前不久在上海下线,C919的综合监视电子系统是由无锡企业研发制造.电子监视系统的核心部件是其中的电子芯片.制备该电子芯片的材料是( )
我国自主研发制造的国产大型客机C919前不久在上海下线,C919的综合监视电子系统是由无锡企业研发制造.电子监视系统的核心部件是其中的电子芯片.制备该电子芯片的材料是( )| A. | 铝 | B. | 硅 | C. | 碳 | D. | 钢 |
查看答案和解析>>
科目: 来源: 题型:解答题
| NO | N2 | CO2 | |
| 起始浓度/mol•L-1 | 0.10 | 0 | 0 |
| 平衡浓度/mol•L-1 | 0.04 | 0.03 | 0.03 |
 ,再次达到平衡测得容器中NO、N2、CO2的浓度值比为5:3:3,则△H<0(填“>”、“=”或“<”).
,再次达到平衡测得容器中NO、N2、CO2的浓度值比为5:3:3,则△H<0(填“>”、“=”或“<”).查看答案和解析>>
科目: 来源: 题型:解答题
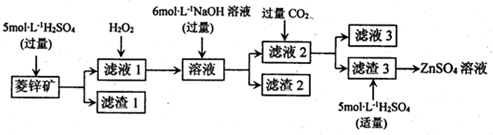
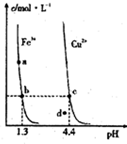 ②常温下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH.金属阳离子浓度的变化如图所示,下列判断正确的是BC.
②常温下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH.金属阳离子浓度的变化如图所示,下列判断正确的是BC.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①和②混合溶液中:c(H+)不变 | |
| B. | ①和④混合溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| C. | ②和③混合溶液中:溶质只有NH4Cl | |
| D. | ③和④分别用等浓度的盐酸中和,消耗盐酸的体积相同 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氯碱工业中NaOH的溶液在阳极区产生 | |
| B. | 电解精炼铜时,阳极质量的减小等于阴极质量的增加 | |
| C. | 铁制品表面镀镍时,镀件做阳极 | |
| D. | 电解法制铝的过程中需不断补充阳极材料(石墨电极) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 合成氨工业温度选择为700K左右,只要是为了提高NH3产率 | |
| B. | 使用催化剂和施加高压,都能提高反应速率,但对化学平衡状态无影响 | |
| C. | 合成氨生产过程中将NH3液化分离,可提高N2、H2的转化率 | |
| D. | 合成氨工业中为了提高氢气的利用率,可适当增加氢气浓度 |
查看答案和解析>>
科目: 来源: 题型:选择题
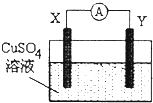
| A. | 若X为Fe,Y为Cu,则铁为正极 | |
| B. | 若X为Ag,Y为Cu,则电流表的指针不发生偏转 | |
| C. | 若X为Cu,Y为Zn,则锌片发生还原反应 | |
| D. | 若X为Fe,Y为C,则碳棒上有红色固体析出 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 明矾净水:Al3++3H2O∧Al(OH)3+3H+ | |
| B. | 氯气通入水中:Cl2+H2O?2H++ClO-+Cl- | |
| C. | 铜和硝酸银溶液反应:Cu+2Ag+═Cu2++2Ag | |
| D. | 稀硫酸与氢氧化钡溶液反应:Ba2++OH-+H++SO42-═H2O+BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com