
科目: 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 向盛有某溶液的试管中滴加NaOH溶液,将湿润的红色石蕊试纸放在试管口 | 试纸未变蓝 | 该溶液中不含NH4+ |
| B | 用高锰酸钾溶液检验乙烯中混有的SO2 | 高锰酸钾溶液褪色 | 乙烯中混有SO2 |
| C | 向氯化钡溶液中通入CO2 | 得到白色沉淀 | 生成了BaCO3 |
| D | 淀粉KI溶液中滴入氯水,再通入SO2 | 先变蓝后褪色 | SO2有还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CO(g) 与Na2O2(s)反应放出509kJ热量时,电子转移数为6.02×1023 | |
| B. | 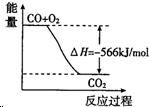 图可表示由CO生成CO2的反应过程和能量关系 | |
| C. | 2Na2O2(s)+2CO2(s)═2Na2CO3(s)+O2(g)△H>-452kJ/mol | |
| D. | CO的燃烧热为283kJ |
查看答案和解析>>
科目: 来源: 题型:解答题
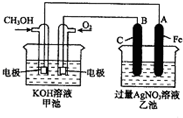 如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O
如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 使酚酞呈红色的溶液:Na+、NH4+、Al3+、NO3- | |
| B. | Kw/c(H+)=0.1 mol•L-1的溶液:Na+、K+、CO32-、ClO- | |
| C. | 含有Fe3+的溶液:Na+、Al3+、Cl-、SCN- | |
| D. | 由水电离产生的c (OH-)=1×10-14 mol•L-1溶液:K+ Na+ Cl- HCO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向某溶液中加入稀硝酸酸化,再滴入BaCl2溶液,产生白色沉淀,则原溶液中一定有SO42- | |
| B. | 向某溶液中加入稀硫酸酸化,再滴入AgNO3溶液,产生白色沉淀,则原溶液中一定有Cl- | |
| C. | 向某溶液中加入碳酸钠溶液,产生白色沉淀,再滴入稀盐酸,沉淀溶解,则原溶液中一定有Ca2+ | |
| D. | 用光洁的铂丝蘸取某无色溶液,在酒精灯外焰里灼烧时观察到黄色火焰,则原溶液中一定有Na+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 应选用100mL容量瓶 | |
| B. | 配置之前容量瓶中残留的蒸馏水会导致浓度偏高 | |
| C. | 定容时腐蚀刻度会导致浓度偏低 | |
| D. | 摇匀、静置后发现凹液面低于刻度线,再加水至刻度线即可 |
查看答案和解析>>
科目: 来源: 题型:解答题
 、④HCHO,其中碳原子采取sp2杂化的分子有①③④(填物质编号),HCHO分子的立体构型为平面三角形.
、④HCHO,其中碳原子采取sp2杂化的分子有①③④(填物质编号),HCHO分子的立体构型为平面三角形.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 某金属元素气态基态原子的逐级电离能的数值分别为738、1451、7733、10540、13630、17995、21703…,当它与氯气反应时生成的阳离子是X3+ | |
| B. | 粗硅$→_{高温}^{Cl_{2}}$SiCl4$→_{高温}^{H_{2}}$Si均能一步实现 | |
| C. | 33gCH≡C-CH=CH-CH3中所含的π键数、12g石墨中所含的碳碳键数均为1.5mol | |
| D. | 灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,可能含有K+ |
查看答案和解析>>
科目: 来源: 题型:解答题
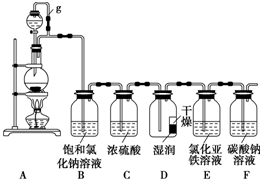
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com