
科目: 来源: 题型:选择题
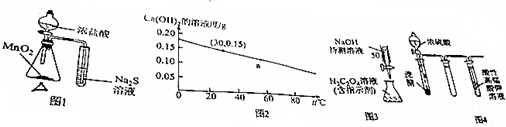
| A. | 图1的装置可用于比较MnO2、Cl2、S的氧化性 | |
| B. | 图2可知:30℃时Ca(OH)2溶液的浓度一定大于60℃时的温度 | |
| C. | 图3的装置可用于已知浓度的H2C2O4溶液测定未知浓度的NaOH溶液 | |
| D. | 图4的实验现象:酸性高锰酸钾溶液中有气泡出现,且溶液颜色逐渐变浅乃至褪去 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 新制氯水、氨水的溶质分别是次氯酸、一水合氨 | |
| B. | 25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | 物质溶于水时,不一定发生化学键的断裂 | |
| D. | 烧碱、冰醋酸、四氯化碳均为电解质 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该有机物不存在 | B. | 该有机物的分子式为C4H4 | ||
| C. | 该有机物的空间构型为正四面体 | D. | 该有机物不属于笨的同系物 |
查看答案和解析>>
科目: 来源: 题型:选择题
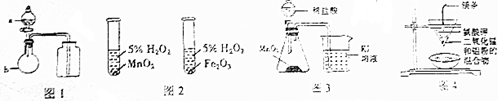
| A. | 用图1所示装置进行浓硫酸与亚硫酸钠的反应制取并收集SO2 | |
| B. | 用图2所示装置进行研究不同催化剂对反应速率的影响 | |
| C. | 用图3所示装置比较MnO2、Cl2、I2的氧化性 | |
| D. | 用图4所示装置可以制取金属锰 |
查看答案和解析>>
科目: 来源: 题型:解答题
 ,B
,B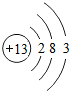 ,二者离子半径:Na+>Al3+(填离子符号).
,二者离子半径:Na+>Al3+(填离子符号).查看答案和解析>>
科目: 来源: 题型:选择题
| A. | (CH3)2=CHCH3和(CH3)2CHCH=CH2 | B. | CH2=C(CH3)2和CH3CH=CHCH3 | ||
| C. | CH3CH2CH2COOH 和CH3COOCH2CH2 | D. | CH3CH2OH和CH3OCH3 |
查看答案和解析>>
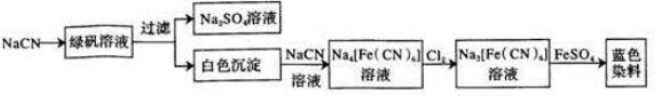
科目: 来源: 题型:解答题

 .
. 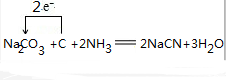 .
.
查看答案和解析>>
科目: 来源: 题型:选择题
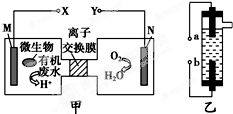
| A. | 装置甲可以在高温环境中工作 | |
| B. | 装置甲中N极发生的电极反应为O2+4H++4e-═2H2O | |
| C. | 装置乙中b极的电极反应式为2H++2e-═H2↑ | |
| D. | 装置乙的a极要与装置甲的Y极连接 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 溶液中溶质微粒一定不带电,胶体中分解质微粒带有电荷 | |
| B. | 溶液呈电中性,胶体带电荷 | |
| C. | 胶体是比溶液更稳定的分散系 | |
| D. | 胶体是一种较稳定的分散系 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com