
科目: 来源: 题型:解答题
 在一密闭容器中发生反应N2+3H22NH3,△H<0达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
在一密闭容器中发生反应N2+3H22NH3,△H<0达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 碳元素的平均相对原子质量 | B. | 碳原子质量 | ||
| C. | 同位素C-12的行相原子质量 | D. | C-12的质量数 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | N2 (g)和O2(g)反应生成NO(g)是放热反应 | |
| B. | 2 molO原子结合生成O2(g)时需要吸收498kJ能量 | |
| C. | N2(g)+O2(g)=2NO(g)的反应热△H=+1444kJ•mol-1 | |
| D. | 1molNO(g)分子中的化学键断裂时需要吸收632kJ能量 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A | H2SO3→H2SO4: | 2H2SO3+O2=2H2SO4 |
| B | Fe→Fe3+: | 2Fe+6H+=2Fe3++3H2↑ |
| C | Br-→Br2: | 2Br-+I2=B r2+2I- |
| D | Cu→CuSO4: | Cu+2H2SO4(稀)=CuSO4+SO2↑+2H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | MO | B. | MO2 | C. | MO3 | D. | M2O3 |
查看答案和解析>>
科目: 来源: 题型:解答题
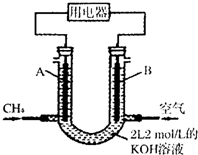 合理利用碳氢化合物以及二氧化碳捕集、存储和转化是当今化学研究的热点问题之一.
合理利用碳氢化合物以及二氧化碳捕集、存储和转化是当今化学研究的热点问题之一.查看答案和解析>>
科目: 来源: 题型:解答题
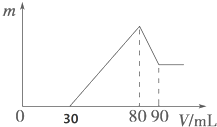 把一定质量的镁、铝混合物投入到1mol•L-1的盐酸中,待金属完全溶解后,向溶液中加入1mol,•L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示.则:
把一定质量的镁、铝混合物投入到1mol•L-1的盐酸中,待金属完全溶解后,向溶液中加入1mol,•L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示.则:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com