
科目: 来源: 题型:选择题
| A. | 浓H2SO4有强氧化性,稀H2SO4完全没有氧化性 | |
| B. | 由于浓H2SO4具有脱水性,所以可用做干燥剂 | |
| C. | 稀硫酸不与铜反应,但把Cu片放在浓H2SO4中立即发生激烈反应 | |
| D. | 在受热的情况下浓硫酸也能与铁、铝发生反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
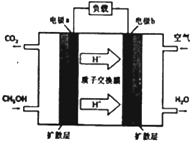 能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
| 实验编号 | T(℃) | $\frac{n(CO)}{n({H}_{2})}$ | P(MPa) |
| 1 | 150 | $\frac{1}{3}$ | 0.1 |
| 2 | A | B | D |
| 3 | 350 | C | 5 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH值 | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
| A. | CO2+H2O+NaClO═NaHCO3+HClO | B. | CO2+H2O+2NaClO═Na2CO3+2HClO | ||
| C. | CH3COOH+NaCN═CH3COONa+HCN | D. | CH3COOH+NaClO═CH3COONa+HClO |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Fe-Zn合金 | B. | Fe-Cu合金 | C. | Fe-Mg合金 | D. | Mg-Al合金 |
查看答案和解析>>
科目: 来源: 题型:解答题
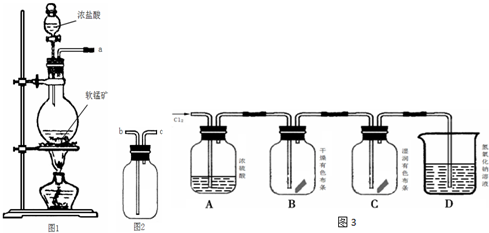
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用闻气味的方法鉴别氢气和氧气 | B. | 用氯化钡溶液鉴别盐酸和稀硫酸 | ||
| C. | 观察气体颜色区别氯气和氧气 | D. | 利用丁达尔效应区别溶液和胶体 |
查看答案和解析>>
科目: 来源: 题型:解答题
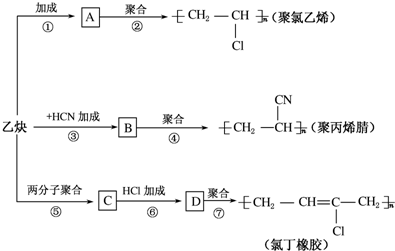

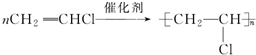 ;
;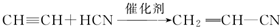 ;
;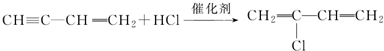 .
.查看答案和解析>>
科目: 来源: 题型:解答题
 实验室用苯和浓硝酸、浓硫酸发生反应制取硝基苯的装置图如图所示.回答下列问题:
实验室用苯和浓硝酸、浓硫酸发生反应制取硝基苯的装置图如图所示.回答下列问题: .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com