
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

| 温度(℃) | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
查看答案和解析>>
科目: 来源: 题型:选择题
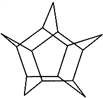 化学家们合成了一种新物质:五星烷,其键线式如图所示.下列关于五星烷的说法中正确的是( )
化学家们合成了一种新物质:五星烷,其键线式如图所示.下列关于五星烷的说法中正确的是( )| A. | 五星烷与己烷互为同系物 | B. | 五星烷的化学式为C15H20 | ||
| C. | 五星烷分子中含有7个五元环 | D. | 五星烷的一氯代物有5种 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该溶液的溶质不可能是NaHSO4 | |
| B. | 向该溶液中加入铝粉,一定能产生大量H2 | |
| C. | 下列离子在该溶液中一定能大量共存:Cl-、K+、Cu2+ | |
| D. | 向该溶液中加入NaHCO3固体,一定有化学反应发生 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1 mol FeI2与足量氯气反应时转移的电子数为2NA | |
| B. | 丙烯和环丙烷组成的42g混合气体中氢原子的个数为6NA | |
| C. | 2 L 0.5 mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| D. | 1 mol Na2O2固体中含离子总数为4NA |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NO2、O2混合气体和H2O | B. | SO2和NaOH溶液 | ||
| C. | NH3和H2O | D. | NO2和H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2SO3已部分被空气中的氧气氧化 | |
| B. | 加入Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4 | |
| C. | 加硝酸后的白色沉淀不一定是BaSO4 | |
| D. | 此实验不能确定Na2SO3是否部分被氧化 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NO3- | B. | HCO3- | C. | Na+ | D. | SO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com