
科目: 来源: 题型:解答题
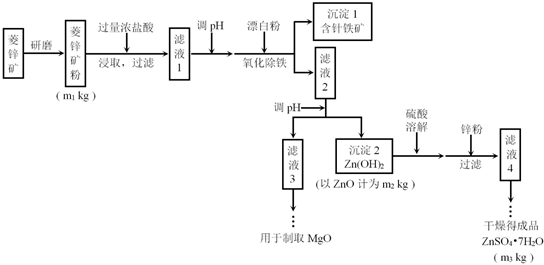
| Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 | |
| 开始沉淀的pH | 10.4 | 6.4 | - | - |
| 沉淀完全的pH | 12.4 | 8.0 | - | - |
| 开始溶解的pH | - | 10.5 | - | - |
| Ksp | 5.6×10-12 | - | 6.8×10-6 | 2.8×10-9 |
查看答案和解析>>
科目: 来源: 题型:解答题
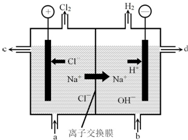 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.
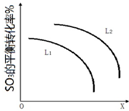
查看答案和解析>>
科目: 来源: 题型:选择题
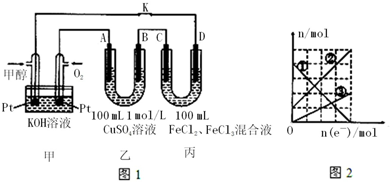
| A. | 负极的电极反应式是:CH3OH-6e-+8OH-═CO32-+6H2O | |
| B. | 乙中A极析出的气体在标准状况下的体积为1.12 L | |
| C. | 右图中②线表示的是Fe2+离子的变化 | |
| D. | 反应结束后,要使丙装置溶液中金属阳离子恰好完全沉淀,需要280 mL 5.0 mol/L NaOH溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子半径:W>Y>Z>X | |
| B. | 气态氢化物的稳定性:Z<X | |
| C. | Y、Z的氧化物都有两性 | |
| D. | Y、W最高价氧化物对应水化物间可以相互反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 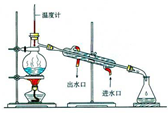 用如图装置分离甲苯和水 | |
| B. | 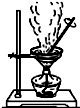 蒸干NH4Cl溶液制备NH4Cl晶体 | |
| C. | 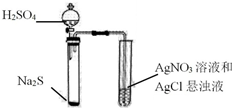 证明Ag2S溶解度小于AgCl | |
| D. | 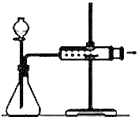 关闭分液漏斗活塞,向外拉动针筒活塞,松开后活塞恢复原位置,证明装置气密性良好 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 少量CO2通入漂白液中:CO2+ClO-+H2O═HClO+HCO3- | |
| B. | 向含K+、CO32-、OH-的溶液中通入少量CO2:2OH-+CO2═CO32-+H2O | |
| C. | 强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4:3ClO-+Fe(OH)3═FeO42-+3Cl-+H2O+4H+ | |
| D. | 3molCl2通入含4molFeI2的溶液中充分反应:2I-+Cl2═I2+2Cl- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在0.1mol/L Na2CO3溶液中,CO32-的数目小于0.1NA个 | |
| B. | 标准状况下,6.0 g乙酸含有0.3 NA个C-H键 | |
| C. | 32gCu与足量硫黄充分反应,转移NA个电子 | |
| D. | 31g白磷(P4)中含有6 NA个共价键 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 木材纤维和土豆淀粉遇碘水均显蓝色 | |
| B. | 食用花生油和鸡蛋清都能发生水解反应 | |
| C. | 包装用材料聚乙烯和聚氯乙烯都属于烃 | |
| D. | 经常使用一次性筷子、纸杯、塑料袋等做法能保护环境 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1828年德国化学家维勒首次在实验室里合成了尿素 | |
| B. | 19世纪初,瑞典化学家贝采利乌斯首次使用“有机”一词,并提出了“有机化学”和“有机化合物”的概念 | |
| C. | 1965年我国科学家人工合成了具有生物活性的蛋白质--结晶牛胰岛素 | |
| D. | 1830年,德国化学家李比希创立了有机化合物的定量分析方法 |
查看答案和解析>>
科目: 来源: 题型:选择题
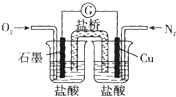
| A. | 石墨的电极反应:O2+2H20+4e-═4OH- | |
| B. | 此装置能将化学能转变为电能 | |
| C. | 电子由Cu电极经导线流向石墨电极 | |
| D. | 电池总反应:2Cu+O2+4HCl═2CuCl2+2H20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com