
科目: 来源: 题型:选择题
| A. | 该反应属于置换反应 | |
| B. | NaH中的H为+1价 | |
| C. | 氧化剂是H2O | |
| D. | 每摩尔NaH参加反应时电子转移数为1e- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 5.6 | B. | 1.6 | C. | 3.2 | D. | 3.6 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 澄清的石灰水与稀盐酸反应 Ca (OH)2+2H+═Ca2++2H2O | |
| C. | 酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+═I2+3H2O | |
| D. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NH4+、NO3-、Al3+、Cl- | B. | K+、SO42-、HCO3-、Na+ | ||
| C. | Mg2+、NO3-、OH-、Na+ | D. | MnO4-、K+、SO42-、Na+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 若质量相等,则质子数一定相等 | B. | 若原子数相等,则中子数一定相等 | ||
| C. | 若分子数相等,则体积一定相等 | D. | 若密度相等,则体积一定相等 |
查看答案和解析>>
科目: 来源: 题型:解答题
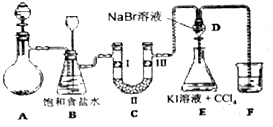
| 选项 | Ⅰ | Ⅱ | Ⅲ |
| A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| B | 干燥的有色布条 | 硅胶 | 湿润的有色布条 |
| C | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| D | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
查看答案和解析>>
科目: 来源: 题型:解答题
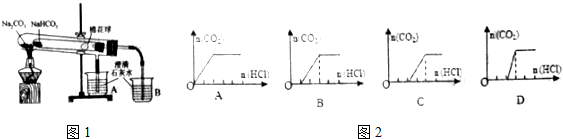
查看答案和解析>>
科目: 来源: 题型:解答题
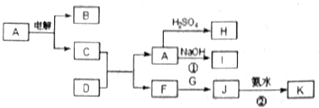
查看答案和解析>>
科目: 来源: 题型:解答题
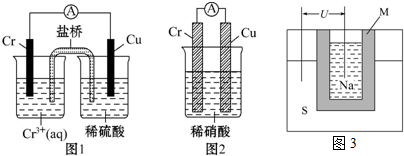
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com