
科目: 来源: 题型:解答题
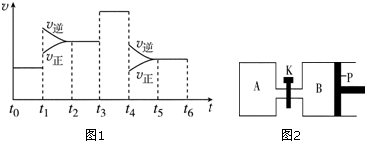
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②③④ | B. | ④⑤⑥ | C. | ②③⑥ | D. | ①③⑤ |
查看答案和解析>>
科目: 来源: 题型:选择题
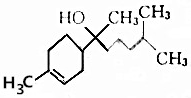
| A. | 分子式为C15H26O | B. | 能和NaHCO3溶液反应生成CO2 | ||
| C. | 不能使酸性高锰酸钾溶液褪色 | D. | 能与乙酸发生取代反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
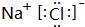 .
.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 有机物在滤液中 | B. | 杂质在滤液中 | C. | 有机物滤纸上 | D. | 杂质在溶剂中 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 自然界中硅元素均以SiO2形式存在 | |
| B. | 高纯度晶体Si可用于制造光导纤维 | |
| C. | 该反应条件下C的还原性比Si强 | |
| D. | 生成4.48LCO时转移电子数为0.4×6.02×1023 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,2.24L甲烷中含氢原子数为0.4NA | |
| B. | 0.3molNO2与足量的水反应转移电子数为0.2NA | |
| C. | 1L0.1mol•L-1Na2CO3溶液中含CO32-数目为0.1NA | |
| D. | 5.6g铁完全溶于足量稀硝酸,转移电子数为0.3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com