
科目: 来源: 题型:选择题
| A. | 在铁质船体上镶嵌锌块,可以减缓船体被海水腐蚀的速率,称为牺牲阴极的阳极保护法 | |
| B. | 电解饱和食盐水是将电能转变成化学能,在阴极附近生成氢氧化钠和氢气 | |
| C. | 铜锌原电池反应中,铜片作正极,产生气泡发生还原反应,电子从铜片流向锌片 | |
| D. | 外加电流的阴极保护法是将被保护的金属与外加电源的正极相连 |
查看答案和解析>>
科目: 来源: 题型:解答题
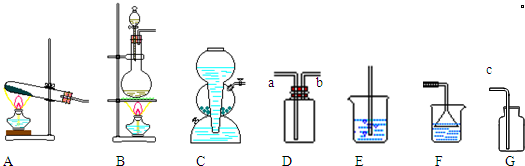
查看答案和解析>>
科目: 来源: 题型:解答题
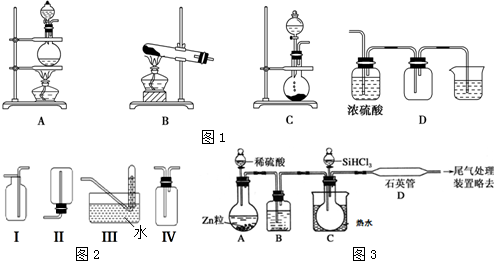
查看答案和解析>>
科目: 来源: 题型:选择题
| X | ||
| Y | Z | W |
| T |
| A. | X、W、Z元素的原子半径依次减小 | |
| B. | Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增 | |
| C. | YX2晶体熔化、液态WX3气化均需克服分子间作用力 | |
| D. | 根据元素周期律,可以推测T2X3具有氧化性和还原性 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Cu→CuSO4 | B. | C→CO2 | C. | CuO→CuSO4 | D. | Fe2O3→Fe2(SO4)3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 上述反应中氧化产物只有N2 | |
| B. | 经测定,NaCN的水溶液呈碱性,说明CN-能促进水的电离 | |
| C. | 若上述反应生成0.4molCO2,则溶液中阴离子增加的物质的量为2mol | |
| D. | 现取1L含CN-1.04mg/L的废水,理论需用4.010-5molCl2处理 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 除去N2中的O2:通过灼热的CuO粉末,收集气体 | |
| B. | 某吸热反应能自发进行,则该反应一定是熵增的反应 | |
| C. |  如图是从化学试剂商店买回的硫酸试剂标签,配制80mL2.3mol•L-1的稀硫酸需量取该硫酸12.5 mL | |
| D. | 下列各种物质在一定条件下反应,所得产物与反应物的用量或与反应条件无关①Na2SiO3+CO2+H2O ②Fe+Cl2 ③Ca(HCO3)2+Ca(OH)2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | B与A只能组成BA3化合物 | |
| B. | 第三周期中,D原子的原子半径最大 | |
| C. | A、B、C三元素不可能形成离子化合物 | |
| D. | E的氧化物对应水化物一定有强的氧化性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com