
科目: 来源: 题型:选择题
| A. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 | |
| B. | 浓硫酸与含有水分的蔗糖作用,不显示酸性 | |
| C. | 鸡蛋白溶液遇到浓硝酸可以变为黄色 | |
| D. | 向装有Fe(NO3)2溶液的试管中加入稀硫酸,在试管口观察到红棕色气体 |
查看答案和解析>>
科目: 来源: 题型:解答题
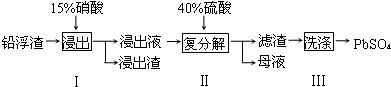
| 化学式 | CaSO4 | Ag2SO4 | PbSO4 |
| Ksp | 4.9×10-5 | 1.2×10-5 | 1.6×10-8 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下,浓H2SO4可以用铝(或铁)容器贮存,说明浓H2SO4与Al(或Fe)常温下不反应 | |
| B. | 在蔗糖中加入浓H2SO4后出现发黑现象,说明浓H2SO4具有脱水性 | |
| C. | 浓H2SO4能使胆矾由蓝变白,说明浓H2SO4具有吸水性 | |
| D. | 稀H2SO4能与Fe反应产生H2,说明稀H2SO4也有氧化性 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在pH=1的溶液中:K+、Na+、SO42-、HCO3- | |
| B. | 在0.1 mol•L-1 Na2CO3溶液中:Al3+、K+、NO3-、SO42- | |
| C. | 在0.1 mol•L-1 FeCl3溶液中:K+、NH4+、I-、SCN- | |
| D. | 在$\frac{c({H}^{+})}{c(OH)}$=10-12的溶液中:K+、Na+、ClO-、NO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HCN的结构式:H-C≡N | |
| B. | HClO的电子式: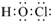 | |
| C. | 中子数为16的硫原子符号为:${\;}_{32}^{16}$S | |
| D. | Na+的离子结构示意图: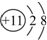 |
查看答案和解析>>
科目: 来源: 题型:解答题
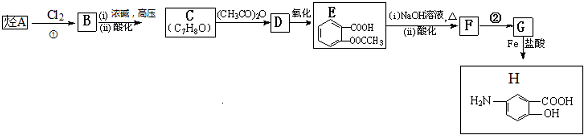
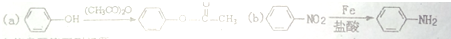
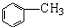 ,F含有的官能团是羧基和酚羟基(填名称).
,F含有的官能团是羧基和酚羟基(填名称).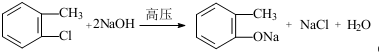 .
.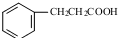 .
.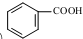 发生取代时,在羧基间位取代;②
发生取代时,在羧基间位取代;②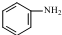 易发生氧化反应.以A为原料合成化合物
易发生氧化反应.以A为原料合成化合物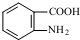 的设计合成路线为(其他试剂任选):
的设计合成路线为(其他试剂任选):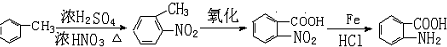 .
.查看答案和解析>>
科目: 来源: 题型:解答题
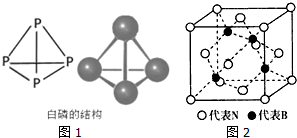 利用周期表中同族元素的相似性,可预测元素的性质.
利用周期表中同族元素的相似性,可预测元素的性质.查看答案和解析>>
科目: 来源: 题型:解答题
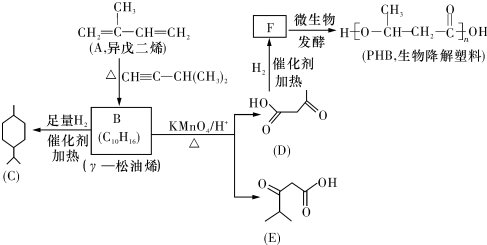
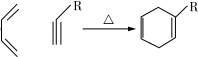
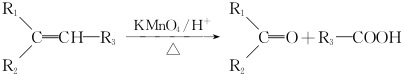
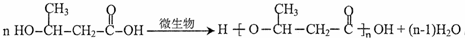 .
.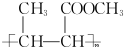 (一种类似有机玻璃的塑料).在催化剂作用下,第三步反应的化学方程式是
(一种类似有机玻璃的塑料).在催化剂作用下,第三步反应的化学方程式是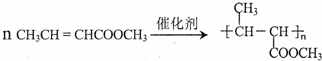 .
.查看答案和解析>>
科目: 来源: 题型:选择题
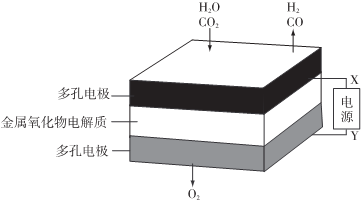
| A. | X是电源的负极 | |
| B. | 阴极的反应式是:H2O+2eˉ═H2+O2- | |
| C. | 总反应可表示为:H2O+CO2═H2+CO+O2 | |
| D. | 阴、阳两极生成的气体的物质的量之比是1:2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2种 | B. | 4种 | C. | 6种 | D. | 8种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com