
科目: 来源: 题型:解答题

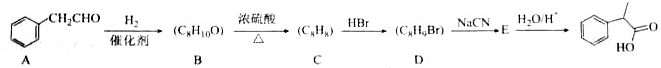
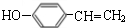 .
.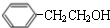 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$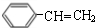 +H2O;C→D的反应类型为加成反应
+H2O;C→D的反应类型为加成反应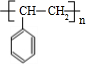 .
.查看答案和解析>>
科目: 来源: 题型:选择题
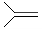 ,脱落酸(如图)可用作植物生长抑制剂,下
,脱落酸(如图)可用作植物生长抑制剂,下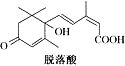 列对该物质的叙述正确的是( )
列对该物质的叙述正确的是( )| A. | 其分子式为C15H22O4 | |
| B. | 其属于芳香族化合物 | |
| C. | 能与氢氧化钠溶液反应,但不能与碳酸氢钠溶液反应 | |
| D. | 该物质在一定条件下可发生自身取代反应生成含七元环的物质. |
查看答案和解析>>
科目: 来源: 题型:选择题
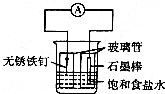 如图为铁的吸氧腐蚀实验装置,下列说法中错误的是( )
如图为铁的吸氧腐蚀实验装置,下列说法中错误的是( )| A. | 右玻璃管内液面高于左玻璃管内液面 | |
| B. | 溶液中的Cl-向铁钉方向移动 | |
| C. | 石墨棒做正极,电极反应式为O2+2H2O+4e-═4OH- | |
| D. | 向插人铁钉的玻璃管内滴人Na0H溶液,可观察到铁钉附近的溶液中有沉淀生成 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | CO2 | B. | BeCl2 | C. | BF3 | D. | XeF2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | e=$\frac{1}{11.2}$mol•L-1、ω=$\frac{36.5}{224ρ}$% | B. | e=$\frac{1}{22.4}$mol•L-1、ω=$\frac{36.5}{224ρ}$% | ||
| C. | e=$\frac{1}{22.4}$mol•L-1、ω=$\frac{36.5}{112ρ}$% | D. | e=$\frac{1}{11.2}$mol•L-1、ω=$\frac{23}{224}$% |
查看答案和解析>>
科目: 来源: 题型:解答题
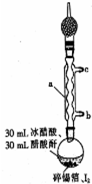 四碘化锡是一种橙红色结晶,熔点为144.5℃,沸点为364℃,不溶于冷水,溶于醇、苯、氯仿等,遇水易水解,常用作分析试剂和有机合成试剂.实验室制备四碘化锡的主要步骤如下:
四碘化锡是一种橙红色结晶,熔点为144.5℃,沸点为364℃,不溶于冷水,溶于醇、苯、氯仿等,遇水易水解,常用作分析试剂和有机合成试剂.实验室制备四碘化锡的主要步骤如下:查看答案和解析>>
科目: 来源: 题型:解答题
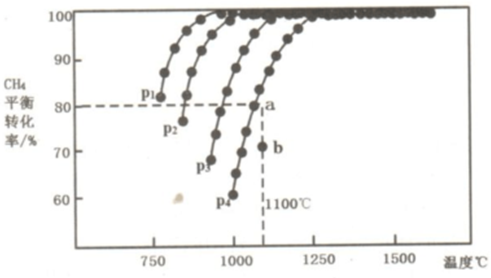
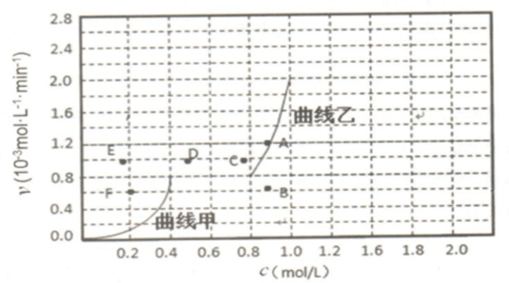
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 22.4L氯气和氢气的混合气体含有2NA个原子 | |
| B. | 0.1mol/L的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA | |
| C. | 标准状况下,22.4L乙烯和丙烯的混合气体中含有的碳原子数目为2.5NA | |
| D. | 1molFeI2与1molCl2反应转移的电子数为2NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2.0gH2O与D2O的混合物中所含中子数为NA | |
| B. | 标准状况下1.4 g乙烯所含共用电子对数为0.25NA | |
| C. | 3 mol单质Fe完全转变为Fe3O4,失去8 NA个电子 | |
| D. | 50ml 12 mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA |
查看答案和解析>>
科目: 来源: 题型:解答题
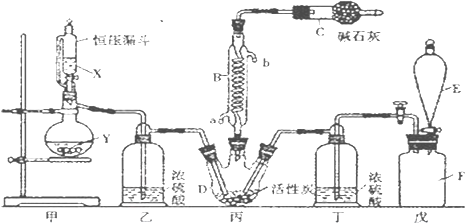
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com