
科目: 来源: 题型:解答题
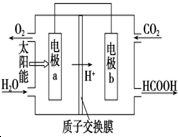 燃料的使用和防污染是社会发展中一个无法回避的矛盾话题.
燃料的使用和防污染是社会发展中一个无法回避的矛盾话题.查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验目的 | 实验方案 |
| A | 检验亚硫酸钠是否变质 | 先将亚酸钠样品溶于水配成溶液,然后加入足量稀盐酸酸化,再加入Ba(NO3)2溶液观察是否生成白色沉淀观察是否产生白色沉淀 |
| B | 除去苯中混有的苯酚 | 加入适量的溴水充分反应后过滤弃去沉淀 |
| C | 除去NaCl晶体中少量的KNO3杂质 | 先将晶体溶于水配成溶液,然后蒸发结晶并趁热过滤弃去滤液 |
| D | 检验CH3CH2Br中存在的溴元素 | 将CH3CH2Br与NaOH溶液共热,冷却后,取出上层水溶液,加入AgNO3溶液,观察是否产生淡黄色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 分别与滴有酚酞的NaOH溶液共热可区别煤油与植物油 | |
| B. | 煤含有苯、甲苯等,先干馏后分馏获可得苯、甲苯等芳香烃 | |
| C. | 在水电离出H+浓度为1×10-12mol/L溶液中一定大量存在Fe2+、Na+、NO3-、Cl- | |
| D. | 在NH4HSO3溶液中加入少量NaOH溶液反应的离子方程式为NH4++OH-=NH3•H2O |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 立方烷属于烷烃 | |
| B. | 立方烷的二氯代物有三种同分异构体 | |
| C. | 立方烷在通常情况下是气体 | |
| D. | 常温下立方烷能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在过氧化钠与水的反应中,每生成0.1mol氧气,转移的电子数目为0.4NA | |
| B. | 氢氧燃料电池正极消耗22.4L气体时,电路中通过的电子数目为4NA | |
| C. | 在30g二氧化硅晶体中含有的共价键数目为2NA | |
| D. | 将常温下含NA个NO2、N2O4分子的混合气体冷却至标准状况,其体积约为22.4L |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 大气中PM2.5比表面积大,吸附力强,能吸附许多有毒有害物质 | |
| B. | 在厨房里可用米汤检验加碘食盐中的碘 | |
| C. | 14C可用于文物年代的鉴定,14C与12C互为同位素 | |
| D. | 喝补铁剂时,加服维生素C效果更好,原因是维生素C具有还原性 |
查看答案和解析>>
科目: 来源: 题型:解答题
 是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如所示:
是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如所示:
 $→_{△}^{H_{2}O/H+}$
$→_{△}^{H_{2}O/H+}$
 .
. $→_{△}^{催化剂}$
$→_{△}^{催化剂}$ +H2O.
+H2O. ,与D互为同分异构体且含有碳碳双键的苯的二取代物有6种,其中核磁共振氢谱为5组峰,且峰面积比为2:1:2:2:1的结构简式是
,与D互为同分异构体且含有碳碳双键的苯的二取代物有6种,其中核磁共振氢谱为5组峰,且峰面积比为2:1:2:2:1的结构简式是 (任写一种).
(任写一种). )的
)的查看答案和解析>>
科目: 来源: 题型:解答题
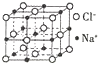 由C、N、O、Na、Fe五种元素组成的配合物Na2[Fe(CN)5(NO)]可用于治疗高血压急症.
由C、N、O、Na、Fe五种元素组成的配合物Na2[Fe(CN)5(NO)]可用于治疗高血压急症.查看答案和解析>>
科目: 来源: 题型:解答题

| 化学键 | S=O(SO2) | O=O(O2) | S=O(SO3) |
| 能量/KJ | 535 | 496 | 472 |

查看答案和解析>>
科目: 来源: 题型:选择题
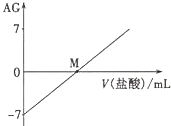 溶液的酸碱性可用酸度(AG)表示,AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.室温下,将0.01mol•L-l盐酸逐滴滴人20.00mL 0.01 mol•L-l氨水中,溶液的AG变化如图所示.下列说法正确的是( )
溶液的酸碱性可用酸度(AG)表示,AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.室温下,将0.01mol•L-l盐酸逐滴滴人20.00mL 0.01 mol•L-l氨水中,溶液的AG变化如图所示.下列说法正确的是( )| A. | 室温下,0.01 mol•L-l盐酸的AG=12 | B. | M点时溶液中:c(NH4+)=c(Cl-) | ||
| C. | M点加入盐酸的体积大于20.00 mL | D. | M点以后NH4+的水解程度逐渐增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com